Sobre la superficie de Dios
Gestes et opinions du docteur Faustroll, pataphysicien. Roman Néo-Scientifique –Gestas y opiniones del doctor Faustroll, patafísico: novela neo-científica– es una obra del dramaturgo y novelista Alfred Jarry (1873-1907).

El libro describe las aventuras del patafísicoi Doctor Faustroll, de su babuino hidrocéfalo Bosse-de-Nage y del oficial de justicia René-Isidore Panmuphle, que aparece en la historia para embargar los bienes de Faustroll.
Esta novela es ‘la biblia’ del Colegio de Patafísicaii, que le ha dedicado diferentes exégesis. El texto está plagado de referencias filosóficas, e incluso matemáticas, en muchas ocasiones usando un lenguaje incoherente.
El Doctor Faustroll es un científico verdaderamente singular. Nacido en Circasia a la edad de 63 años –y fallecido ese mismo año– es pionero de la patafísica y curador perpetuo del Colegio de Patafísica desde 1947.
La historia comienza con el desalojo del Doctor Faustrollde su residencia. Junto a Bosse-de-Nage y René-Isidore Panmuphle, el científico realiza un ‘viaje de París a París por mar’, viaje que le conduce a la muerte. Proyectado dentro de la ‘Ethernidad’, Faustroll transmite –a través de una carta telepática– a Lord Kelvin diferentes reglas sobre el tiempo, el Sol, el espacio, etc. También traduce al matemático y astrónomo Hipócrates de Quíos –al que Jarry atribuye el origen de la patafísica– y, para finalizar, calcula la superficie de Dios, concluyendo el libro con la contundente sentencia ‘La Patafísica es la ciencia’.
El libro está dividido en cuarenta y un capítulos distribuidos en ocho ‘libros’:
-
Procédure (Introducción)
-
Éléments de pataphysique (Elementos de patafísica)
-
De Paris à Paris par mer, ou le Robinson belge (De París a París por mar, o el Robinson belga)
-
Céphalorgie (Cefalorgia)
-
Officiellement (Oficialmente)
-
Chez Lucullus (En casa de Lúculo)
-
Khurmookum
-
Éthernité (Ethernidad)
Se reproduce debajo el último capítulo –traducido por la autora de esta anotación– en el que se calcula la ‘superficie de Dios’.
XLI
SOBRE LA SUPERFICIE DE DIOS
Por definición, Dios no posee extensión pero nos permitimos, por la claridad de nuestro enunciado, suponerle un número cualquiera, mayor que cero, de dimensiones, aunque no tenga ninguna si estas dimensiones desaparecen en los dos miembros de nuestras identidades. Nos conformaremos con dos dimensiones, para poder representar fácilmente figuras de geometría plana sobre una hoja de papel.
Simbólicamente se representa a Dios por un triángulo, pero las tres Personas no deben considerarse como los vértices o las aristas. Son las tres alturas de otro triángulo equilátero circunscrito en el tradicional. Esta hipótesis concuerda con las revelaciones de Anne-Catherine Emmerick, quien vio la cruz (que consideramos como símbolo del Verbo de Dios) en forma de Y, y sólo lo explica por esta razón física: ningún brazo de longitud humana podría extenderse hasta los clavos de las ramas de una tau.
Por lo tanto, POSTULADO:
Hasta tener más información y por nuestra comodidad provisional, suponemos a Dios en un plano y bajo la figura simbólica de tres rectas iguales, de longitud a, pasando por un mismo punto y formando entre ellas ángulos de 120 grados. Es del espacio comprendido entre ellas, o del triángulo obtenido uniendo los tres puntos más alejados de estas rectas, del que nos proponemos calcular el área.
Sea x la mediana prolongación de una de las Personas a, 2y el lado del triángulo al que es perpendicular, N y P las prolongaciones de la recta (a+x) en los dos sentidos hacia el infinito.
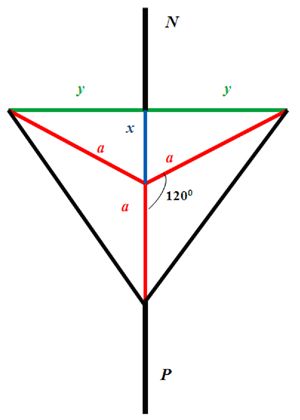 Esta figura –realizada por la autora de la anotación– no aparece en el libro de Jarry: se inserta solo para aclarar las notaciones.
Esta figura –realizada por la autora de la anotación– no aparece en el libro de Jarry: se inserta solo para aclarar las notaciones.Tenemos:
x=∞−N−a−P.
Ahora bien
N=∞−0.
y
P=0.
De donde
x=∞−(∞−0)−a−0=∞−∞+0−a−0
x=−a.
Por otro lado, el triángulo rectángulo cuyos lados son a, x e y nos da:
a²=x²+y².
Así, sustituyendo x por su valor (−a)
a²=(−a²)+y²=a²+y².
De donde
y²=a²−a²=0
e
y=√0.
Así la superficie del triángulo equilátero que tiene por bisectrices de sus ángulos las tres rectas a será:
S=y(x+a)=√0(−a+a)
S=0√0.
COROLARIO.- A primera vista del radical √0, podemos afirmar que el área calculada es a lo más una línea; en segundo lugar, si construimos la figura según los valores obtenidos para x e y, observamos:
Que la recta 2y, que ahora sabemos que va a ser 2√0, tiene su punto de intersección sobre una de las rectas aen sentido inverso de nuestra primera hipótesis, ya que x=−a; y que la base de nuestro triángulo coincide con su vértice;
Que las dos rectas a forman con la primera ángulos menores al menos de 60°, y más aún no pueden encontrar 2√0 más que coincidiendo con la primera recta a.
Esto concuerda con el dogma de equivalencia de las tres Personas entre ellas y a su suma.
Podemos decir que a es una recta que une 0 con ∞, y definir Dios:
DEFINICIÓN.- Dios es el camino más corto entre cero e infinito.
¿En qué sentido?, nos preguntaremos.
– Responderemos que Su nombre no es Julio, sino Más-y-Menos. Y debe decirse:
± Dios es el camino más corto de 0 a ∞, en un sentido o en el otro.
Esto concuerda con la creencia en los dos principios; pero es más exacto atribuir el signo + al de la creencia del sujeto.
Pero como Dios no posee extensión, no es una línea.
– Observemos en efecto que, según la identidad
∞−0−a+a+0=∞
la longitud a es nula, a no es una línea, sino un punto.
Así, definitivamente:
DIOS ES EL PUNTO TANGENTE DE CERO Y DEL INFINITO.
La Patafísica es la ciencia…
 Alfred Jarry en bicicleta. Imagen: Wikimedia Commons.
Alfred Jarry en bicicleta. Imagen: Wikimedia Commons.
Parece que este singular cálculo se inspira en el último capítulo del último libro de Pantagruel de François Rabelais. Allí se afirma que: ‘Esa esfera intelectual, cuyo centro está en todas partes y la circunferencia en ninguna, que llamamos Dios’.
Nota:
Por si alguien se encuentra un tanto confundido, los cálculos realizados no se basan en las matemáticas, sino en la patafísica… ‘la ciencia’…
Más información:
-
La obra completa en el repositorio Gallica
i La patafísica –contracción de epí ta metá ta physiká, es decir, «lo que está alrededor de lo que está más allá de la física»– es un movimiento cultural francés de la segunda mitad del siglo XX vinculado al surrealismo. Toma su nombre de las Gestas y opiniones del doctor Faustroll, patafísico, de Alfred Jarry. Basándose en esta novela, algunas personas comenzaron a practicar la ciencia paródica denominada patafísica que se dedicaba «al estudio de las soluciones imaginarias y las leyes que regulan las excepciones».
ii El Colegio de Patafísica fue fundado en París en 1948 como contraposición caricaturesca a Academias de Arte y Ciencias como el Collège de France y en honor al doctor Faustroll.
Sobre la autora: Marta Macho Stadler es profesora de Topología en el Departamento de Matemáticas de la UPV/EHU, y colaboradora asidua en ZTFNews, el blog de la Facultad de Ciencia y Tecnología de esta universidad.
El artículo Sobre la superficie de Dios se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Blaise Pascal, Dios y la cicloide
- La característica de Euler de una superficie: un invariante topológico
- Coloquios escépticos: ¿hijos de dios?, con Francisco Mora
El modelo de Bohr-Sommerfeld y las propiedades químicas de los elementos
 Foto: Joel Filipe / Unsplash
Foto: Joel Filipe / UnsplashEn el modelo de Bohr (1913) los átomos de los diferentes elementos difieren en la carga y la masa de sus núcleos y en el número y disposición de los electrones. En 1916 Arnold Sommerfeld generalizó el modelo modificando las órbitas electrónicas [1]: ahora ya no eran solo circulares, también podían ser elípticas; y ya no eran como una serie de anillos concéntricos en un plano, sino figuras geométricas en tres dimensiones. ¿Cómo explica este modelo de Bohr-Sommerfeld las propiedades químicas de los elementos?
Los elementos hidrógeno (número atómico Z = 1) y litio (Z = 3) son algo similares químicamente. Ambos tienen valencia 1. Ambos entran en compuestos de estructura similar, por ejemplo, cloruro de hidrógeno (HCl) y cloruro de litio (LiCl). También hay algunas similitudes en sus espectros. Todo esto sugiere que el átomo de litio se parece al átomo de hidrógeno en algunos aspectos importantes. Bohr especuló que dos de los tres electrones del átomo de litio están relativamente cerca del núcleo, en órbitas que se asemejan a las del átomo de helio (Z = 2), formando lo que se puede describir como una «capa» alrededor del núcleo. Pero el tercer electrón está en una órbita circular o elíptica fuera del sistema interno. Dado que este sistema interno consiste en un núcleo de carga +3e y dos electrones, cada uno de los cuales tiene carga –e, su carga neta es +e. Por lo tanto, el átomo de litio puede representarse aproximadamente con un núcleo central de carga +e. Alrededor de este núcleo gira un electrón, algo así como si fuera un átomo de hidrógeno. Esta estructura física similar sería entonces la razón del comportamiento químico similar de hidrógeno y litio.
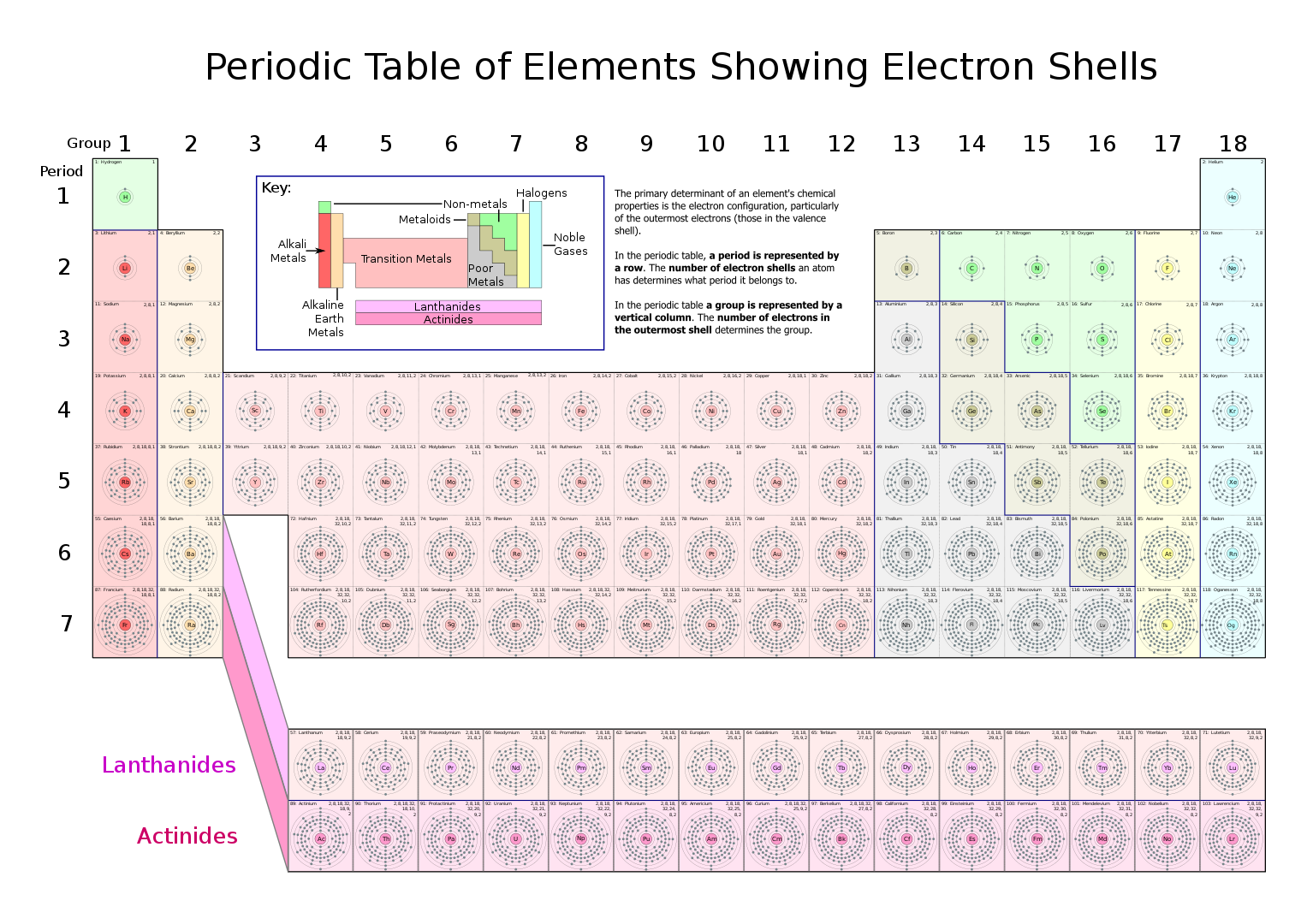 Tabla periódica de Werner-Paneth en la que aparece infográficamente la estructura de capas. Una infografía es una representación inteligible de la información, no la realidad. Fuente: Wikimedia Commons
Tabla periódica de Werner-Paneth en la que aparece infográficamente la estructura de capas. Una infografía es una representación inteligible de la información, no la realidad. Fuente: Wikimedia CommonsEl helio (Z = 2) es un gas noble, químicamente inerte [2]. Estas propiedades indican que el átomo de helio debe ser altamente estable y que tiene sus dos electrones estrechamente unidos al núcleo [3]. Parece sensato, entonces, considerar que ambos electrones se mueven en la misma «capa» más interna cuando el átomo no está excitado. Además, debido a que el átomo de helio es tan estable y químicamente inerte, podemos suponer razonablemente que esta capa no puede contener más de dos electrones. Esta capa se llama K [4]. El único electrón del hidrógeno también está en la capa K cuando el átomo no está excitado. El litio tiene dos electrones en la capa K, llenándola completamente; el tercer electrón inicia una nueva capa, llamada L [4]. Este único electrón externo y débilmente ligado es la razón por la cual el litio se combina tan fácilmente con el oxígeno, el cloro y muchos otros elementos.
El sodio (Z = 11) es el siguiente elemento en la tabla periódica que tiene propiedades químicas similares a las del hidrógeno y el litio. Esta similitud sugiere que el átomo de sodio también es similar al hidrógeno al tener un núcleo central sobre el que gira un electrón. Además, así como el litio sigue al helio en la tabla periódica, el sodio sigue al gas noble neón (Z = 10). Podemos suponer que dos de los diez electrones del neón están en la primera capa (K), mientras que los ocho electrones restantes están en la segunda capa (L). Debido a que es químicamente inerte [2] y la estabilidad del neón, podemos suponer además que estos ocho electrones llenan la capa L hasta su capacidad. Para el sodio, entonces, el undécimo electrón debe estar en una tercera capa, llamada la capa M [4].
Si pasamos al potasio (Z = 19), el siguiente elemento del mismo grupo de la tabla periódica, podemos volver a imaginar un núcleo interno y un solo electrón fuera de él. El núcleo consta de un núcleo con carga +19e. Hay dos, ocho y ocho electrones que ocupan las capas K, L y M, respectivamente. El decimonoveno electrón gira alrededor del núcleo en una cuarta capa, llamada N. El átomo del gas noble argón, con Z = 18, aparece justo antes del potasio en la tabla periódica. El argón nuevamente tiene una estructura de electrones firme y estable, con dos en la capa K, ocho en la capa L y ocho en la capa M.
Parece que tenemos un patrón y que la cosa funciona. ¿Podremos construir todo el sistema de periodos usando solo el modelo de Bohr-Sommerfeld?
Notas:
[1] También introdujo velocidades relativistas para el electrón y determinó que las capas posteriores a la primera pueden tener subcapas, lo que introduciría un nuevo número cuántico. Pero esto ya lo contaremos en otra parte.
[2] A todos los efectos prácticos que nos interesan aquí.
[3] Ya que la química depende del intercambio de electrones. Si el átomo no reacciona químicamente es porque no intercambia sus electrones y esto se debe a que el núcleo los agarra con fuerza. Esto es una sobresimplificación, pero, por ahora, nos sirve.
[4] Los nombres de las capas vienen de la espectroscopía. No les busques lógica porque no la tienen más allá del orden alfabético. Tienen historia, pero es irrelevante ahora.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
El artículo El modelo de Bohr-Sommerfeld y las propiedades químicas de los elementos se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- El modelo de Bohr explica las regularidades en el espectro del hidrógeno
- El modelo de Bohr explica la fórmula de Balmer
- El tamaño del átomo de hidrógeno
La evolución nos dice que es probable que seamos la única vida inteligente del universo
 NASA
NASA¿Estamos solos en el universo? La pregunta que se plantea es si la inteligencia es un resultado probable de la selección natural o un improbable golpe de suerte. Por definición, los acontecimientos probables se producen con frecuencia, mientras que los sucesos improbables tienen lugar pocas veces o una sola vez. La historia de nuestra evolución muestra que muchas adaptaciones de carácter crucial –no solo la inteligencia, sino también los animales y las células complejas, la fotosíntesis y la propia vida– fueron sucesos únicos y excepcionales y, por tanto, muy improbables. Nuestra evolución tal vez haya sido como ganar la lotería… solo que con una probabilidad mucho menor.
El universo es inmensamente grande. La Vía Láctea tiene más de 100 000 millones de estrellas, y en el universo observable, es decir, en la diminuta fracción de universo que podemos ver, hay más de un billón de galaxias. Aunque los mundos habitables son escasos, el número por sí solo —existen tantos planetas como estrellas, puede que más— invita a pensar que hay mucha vida ahí fuera. Si es así, ¿dónde se ha metido? Esta es la paradoja de Fermi. El universo es inmenso y viejo, y dispone de tiempo y espacio suficiente para que la inteligencia evolucione; sin embargo, no hay pruebas de que tal cosa ocurra.
¿Cabría pensar, sencillamente, que a lo mejor es poco probable que la inteligencia evolucione? Por desgracia, no podemos estudiar la vida extraterrestre para responder a esta pregunta. Pero sí podemos estudiar los casi 4 500 millones de años de historia que tiene la Tierra y observar cuándo se repite –o no– la propia evolución.
A veces la evolución se repite, de tal forma que pueden observarse especies diferentes que evolucionan de manera convergente hacia resultados similares. Si la propia evolución se repite con frecuencia, nuestra evolución podría ser un acontecimiento probable, incluso inevitable.
 El tilacino, parecido al lobo.
El tilacino, parecido al lobo.Wikipedia
De hecho, existen ejemplos notables de convergencias evolutivas. El tilacino de Australia, también conocido como lobo marsupial o tigre de Tasmania, hoy extinguido, tenía una bolsa semejante a la de los canguros, pero, por lo demás, parecía un lobo, a pesar de que evolucionó a partir de un linaje de mamíferos diferente. También hay topos marsupiales, marsupiales hormigueros y ardillas planeadoras marsupiales. Es sorprendente comprobar cómo toda la historia evolutiva de Australia, con la diversificación que experimentaron sus mamíferos tras la extinción de los dinosaurios, es paralela a la de otros continentes.
Otros casos llamativos de convergencia son el delfín y el extinto ictiosaurio, que evolucionaron de forma similar para deslizarse por el agua, así como las aves, los murciélagos y los pterosaurios, que evolucionaron de manera convergente para volar.
 Ojo de calamar.
Ojo de calamar.PLoS Biology
También se observan convergencias en órganos independientes. Los ojos evolucionaron no solo en los vertebrados, sino también en los artrópodos, los pulpos, los gusanos y las medusas. Los vertebrados, los artrópodos, los pulpos y los gusanos, cada uno por su cuenta, desarrollaron mandíbulas. Por su parte, las patas evolucionaron de forma convergente en los artrópodos, los pulpos y cuatro tipos de peces (tetrápodos, peces sapo, rájidos, peces del fango).
Aquí está la trampa. Toda esta convergencia tuvo lugar dentro de un mismo linaje, los eumetazoos, que son animales complejos dotados de simetría, boca, tubo digestivo, músculos y un sistema nervioso. Hubo eumetazoos diferentes que desarrollaron soluciones similares a problemas similares, pero la compleja estructura corporal que lo hizo posible es única. Los animales complejos evolucionaron una sola vez en la historia de la vida, lo que da a entender que son improbables.
Sorprende constatar que muchos acontecimientos fundamentales de la historia de nuestra evolución son únicos y, seguramente, improbables. Uno es el esqueleto óseo de los vertebrados, que permitió que los animales grandes se desplazaran hacia la tierra. Las complejas células eucariotas de las que están compuestos todos los animales y plantas, y que contienen núcleos y mitocondrias, evolucionaron una sola vez. El sexo evolucionó una única vez. La fotosíntesis, que aumentaba la energía disponible para la vida y producía oxígeno, es un acontecimiento único. A este respecto, también lo es la inteligencia humana. Existen lobos y topos marsupiales, pero no hay humanos marsupiales.
 El esqueleto de los vertebrados es único.
El esqueleto de los vertebrados es único.Smithsonian Institution
Hay lugares donde la evolución se repite y otros donde no. Si solo nos fijamos en la convergencia, se crea un sesgo de confirmación. La convergencia parece ser la norma y nuestra evolución se presenta como algo probable. Sin embargo, cuando se presta atención a la no convergencia, se observa que está en todas partes, y las adaptaciones decisivas y complejas parecen ser las que menos se repiten, por lo que adquieren carácter improbable.
Además, estos acontecimientos dependían unos de otros. Los seres humanos no pudieron evolucionar hasta que los peces desarrollaron huesos que les permitieron arrastrarse hasta la tierra. Los huesos no pudieron evolucionar hasta que aparecieron los animales complejos. Los animales complejos necesitaban células complejas, y las células complejas necesitaban oxígeno, producido por la fotosíntesis. Nada de esto sucede sin la evolución de la vida, un acontecimiento singular entre acontecimientos singulares. Todos los organismos provienen de un solo antepasado; por lo que sabemos, la vida ocurrió una sola vez.
Es curioso observar que todo este proceso requiere un tiempo sorprendentemente largo. La fotosíntesis evolucionó 1 500 millones de años después de la formación de la Tierra; las células complejas, tras 2 700 millones de años; los animales complejos, al cabo de 4 000 millones de años; y la inteligencia humana, 4 500 millones de años después de que se formara la Tierra. El hecho de que estas innovaciones sean tan útiles pero tardaran tanto en evolucionar implica que son increíblemente improbables.
Una sucesión improbable de acontecimientos
Es posible que estas innovaciones puntuales, casualidades de importancia crucial, crearan una cadena de obstáculos o filtros evolutivos. De ser así, nuestra evolución no fue como ganar la lotería; fue como ganar la lotería una vez y otra y otra y otra. En otros mundos, es posible que estas adaptaciones decisivas hubieran evolucionado demasiado tarde para que la inteligencia apareciera antes de que sus soles se convirtieran en novas, o que no hubieran evolucionado en absoluto.
Supongamos que la inteligencia depende de una cadena de siete innovaciones improbables –el origen de la vida, la fotosíntesis, las células complejas, el sexo, los animales complejos, los esqueletos y la propia inteligencia–, y que cada una tiene un 10 % de posibilidades de evolucionar. Las probabilidades de que la inteligencia evolucione pasan a ser 1 entre 10 millones.
 La fotosíntesis, otra adaptación única.
La fotosíntesis, otra adaptación única.Nick Longrich
Pero las adaptaciones complejas podrían ser incluso menos probables. La fotosíntesis necesitó una serie de adaptaciones en cuanto a proteínas, pigmentos y membranas. Los animales eumetazoos requirieron de múltiples innovaciones anatómicas (nervios, músculos, boca). Por tanto, es posible que cada una de estas siete innovaciones cruciales evolucione solo el 1 % de las veces. En tal caso, la inteligencia evolucionará solamente en 1 de cada 100 billones de mundos habitables. Teniendo en cuenta que los mundos habitables son escasos, podríamos ser la única vida inteligente de la galaxia, o incluso del universo observable.
Así y todo, estamos aquí, y este hecho tiene que valer para algo, ¿no? Si la evolución tiene suerte 1 de cada 100 billones de veces, ¿cuáles son las probabilidades de que nos hallemos en un planeta donde la evolución tuvo lugar? En realidad, las probabilidades de estar en ese mundo improbable son del 100 %, porque no podríamos tener esta conversación en un mundo donde la fotosíntesis, las células complejas o los animales no evolucionaran. Es el principio antrópico. La historia de la Tierra tiene que haber permitido que la vida inteligente evolucionara, pues, de lo contrario, no estaríamos aquí para plantearnos estas cuestiones.
La inteligencia depende, al parecer, de una cadena de acontecimientos improbables. Pero teniendo en cuenta la enorme cantidad de planetas, e igual que un número infinito de monos que golpean un número infinito de máquinas de escribir para redactar Hamlet, está destinada a evolucionar hacia alguna parte. El resultado improbable fuimos nosotros.![]()
Sobre el autor: Nick Longrich es profesor titular (senior lecturer) en el departamento de paleontología y biología evolutiva de la University of Bath
Este artículo fue publicado originalmente en The Conversation. Artículo original.
El artículo La evolución nos dice que es probable que seamos la única vida inteligente del universo se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- La evolución de la vida inteligente: ¿Azar o necesidad?
- Vida alienígena inteligente, una historia terráquea
- El universo en un día: Vida y diversidad, por Carlos Chordá
Breve historia de las ciencias del clima
 Imagen de Arek Socha / Pixabay
Imagen de Arek Socha / Pixabay
La climatología es una ciencia peculiar: no hay que confundirla con la meteorología. Por una parte, se considera una rama de las ciencias atmosféricas, y por tanto perteneciente a las ciencias físicas. Por otro lado, se trata de un subcampo de la geografía perteneciente a las llamadas Ciencias de la Tierra. Sin embargo, la climatología también incluye aspectos de la oceanografía y la biogeoquimica, al igual que de otras ciencias como la geofísica, la glaciología, ecología, ciencias computacionales, meteorología, la economía y… también la historia. Y es que el clima, como es natural, está presente en nuestro planeta mucho antes que la especie humana. Es a lo que se dedica la paleoclimatología, que entre otras cosas trata de hacer arqueología de fósiles u otros signos que permitan comprender cómo fueron los climas a lo largo de la historia de la Tierra.
Hoy en día, la ciencia climática utiliza modelos computacionales que permiten estudiar la evolución del clima e, incluso, realizar proyecciones de cómo será en el futuro. No hay duda de que esta ciencia ha cobrado una gran relevancia social, especialmente desde que la concienciación medioambiental se hizo presente en el debate público durante la segunda mitad del siglo XX. De hecho, la historia que tiene detrás muestra que, en realidad, nunca ha sido una disciplina bien definida y que probablemente no existiría de no ser por los aspectos sociales, culturales y tecnológicos que contingentemente la han llevado a coronarse como una de las ciencias de mayor impacto en la vida diaria actual de muchas personas.
 Fuente: Wikimedia Commons
Fuente: Wikimedia CommonsEn la época clásica, por “clima” se entendía una cosa bien distinta a lo que hoy conciben los climatólogos. Su significado estaba acotado a cuestiones de geografía, un invento de los trabajos de cartografía del siglo III a.C en la Grecia Antigua. No tenía prácticamente nada que ver con la meteorología o la atmósfera, pues hablar del “clima” de un lugar era equivalente a dar sus coordenadas geográficas más que explicar si hacía frío o calor, su humedad o la frencuencia con que llovía en la zona. De hecho, el término “clima” proviene del griego (κλίμα) y significa “zona” o “lugar”.
El concepto “clima” tuvo que esperar hasta el siglo XVIII, momento en el que fue definido como la media de los estados meteorológicos en un lugar a lo largo del tiempo. Sin embargo, sólo se volvió un objeto de la práctica científica cuando los servicios meteorológicos nacionales pudieron proveerse de grandes cantidades de datos para hacer estadística con ellos, lo cual no ocurrió hasta mediados del siglo XIX.
Esta concepción física del clima vino, además, de la mano de la hipótesis científicas del cambio climático. Antes, los colonos del siglo XVII ya auguraban variaciones antropogénicas en el tiempo, cuando en sus observaciones metereológicas se daban cuenta de cambios en zonas particulares. Ellos los atribuían a sus esfuerzos en el cultivo de la tierra, para lo cual tenían que transformar los ecosistemas y, de algún modo, sospechaban que eso tenía su impacto en la meteorología. No obstante, no era una discusión científica, sino más bien una preocupación por la prosperidad de sus cultivos.
 Fuente: Wikimedia Commons
Fuente: Wikimedia CommonsFue con la entrada de la segunda mitad del siglo XVIII cuando empezaron a emerger los debates científicos acerca de si realmente existía un cambio climático y, de existir, cuáles podrían ser las causas de este. La emergencia y desarrollo de la climatología moderna, en sintonía con las nuevas ciencias surgidas con la Revolución Científica, había empezado a aplicar la metodología y formalismos propias de la nueva forma de conocimiento. La matematización y la experimentación eran piezas claves a la hora de comprender científicamente el mundo, y ello llegó al estudio del clima a través de las nuevas teorías de la distribución del calor y la humedad, que reemplazaron a la antigua astrometeorología. El clima empezó a ser estudiado en dimensiones más extensas y escalas temporales más amplias, especialmente cuando descubrieron las eras glaciares pasadas y la discusión de sus causas empezó a cobrar importancia.
Todas esas investigaciones que llevaron científicos como Fourier, Tyundall o Arrhenius, se vieron radicalmente aceleradas a lo largo del siglo XX, sobre todo en su segunda mitad. Hasta entonces, el imperalismo europeo y estadounidense hizo que la climatología se centrara en las geografías pendientes de exploración y zonas concretas de interés, aparte de que la instrumentación disponible no permitía grandes avances ante un objeto tan inmenso y complejo. Sin embargo, entrado el siglo XX el clima se empieza a poder concebir como una entidad global, como una entidad planetaria. Ello vino de la mano de los primeros modelos computacionales, junto con la aparición de otras tecnologías como los satélites artificiales, el radar, los espectómetros, las radiosondas y, en general, la tecnología computacional. Las nuevas capacidades instrumentales permitieron investigar las capas más altas de la atmósfera y mejorar el entendimiento de la física de los procesos atmosféricos. Junto a la información proporcionada por satélites artificiales y la red distribuida de centros meteorológicos, los climatólogos empezaron a tener una visión de conjunto y el clima pasó a convertirse en un objeto científico de escala planetaria.
La actividad climatológica también se transformó por influencia de los cambiantes contextos políticos y culturales durante las guerras mundiales y la guerra fría y, a partir de 1970, por el medioambientalismo y la emergencia de los intereses medioambientales. No sólo apareció una nueva ciencia del clima, sino que también acontenció un nuevo problema político, social y cultural en todas las dimensiones de su práctica. Aparecieron instituciones sin precedentes, como el IPCC, encargada de informar con conocimiento científico a las políticas medioambientales. Así, el consenso científico sobre el calentamiento global antropogénico empezó a consolidarse y los intereses y objetivos de la climatología pasaron a tener un uso político y anticipatorio a problemas medioambientales, marginando los enfoques y preocupaciones de esa misma ciencia durante la preguerra.
 Fuente: Wikimedia Commons
Fuente: Wikimedia CommonsAlgunos autores han denominado a este tipo de ciencia como ciencia posnormal, una modalidad de ciencia en la que hay valores en disputa, altos riesgos y decisiones urgentes. Una etapa de la ciencia donde se cuestiona su metodología, su producción y su uso. La compleja relación entre ciencia y política, la comunicación de la incertidumbre o la evaluación de la calidad son nuevos elementos que hacen tan particular a esta actividad científica, que no ha de confundirse con la meteorología. Una estudia el tiempo a corto plazo. La otra cuánto plazo queda para que se nos acabe el tiempo.
Referencias:
Heymann, M., G. Gramelsberger, M. Mahony (Eds.) (2017): Cultures of Prediction in Atmospheric and Climate Sciecne: Epistemic and Cultural Shifts in Computer-based Modelling and Simulation, New York: Routledge.
Funtowicz, S., J. Ravetz (1993): “Science for the post-normal age”, Futures, Vol 25, Issue 7, pp. 739-755.
White, S., C. Pfister, F. Mauelshagen (Eds.) (2018): The Palgrave Handbook of Climate History, London: Palgrave McMillan.
Winsberg, E. (2018): Philosophy and Climate Science, Cambridge (UK): Cambridge University Press.
Sobre el autor: José Luis Granados Mateo (@JoisDo) desarrolla una tesis doctoral en Historia y Filosofía de la Ciencia en la UPV/EHU, becado por la Dirección de Medio Ambiente de la Diputación Foral de Gipuzkoa.
El artículo Breve historia de las ciencias del clima se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Una breve historia del método de la hipótesis
- Una breve historia del concepto de trastorno bipolar
- Breve historia del trastorno bipolar (II): neurobiología y tratamiento
La letra pequeña de algunos métodos de aprendizaje
Vitoria-Gasteiz acogió por primera vez el pasado 18 de octubre el evento Las pruebas de la educación, una jornada que abordó diversos temas educativos desde la evidencia científica. El acto, organizado por el Consejo Escolar de Euskadi y la Cátedra de Cultura Científica de la UPV/EHU, tuvo lugar en el Salón de Actos del Centro de Investigación Micaela Portilla, ubicado en el Campus de la capital alavesa de la UPV/EHU.

La jornada consta de un total de cinco charlas que tratan temas como el rendimiento académico, los métodos de aprendizaje y la innovación educativa, entre otros. La dirección del seminario corre a cargo de la doctora en psicología Marta Ferrero.
En esta primera charla es precisamente Marta Ferrero quien aborda algunas ideas erróneas que existen sobre la educación en el profesorado y revisa los estudios existentes sobre la eficacia de diferentes métodos educativos. En este sentido, el objetivo de la ponencia es “leer detenidamente la letra pequeña” de dos métodos actualmente muy extendidos en las aulas: el aprendizaje basado en proyectos y la aplicación de intervenciones inspiradas en la teoría de las inteligencias múltiples para la adquisición de nuevos aprendizajes.
Edición realizada por César Tomé López a partir de materiales suministrados por eitb.eus
El artículo La letra pequeña de algunos métodos de aprendizaje se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- El error como ocasión de aprendizaje
- Del mito al hecho: hemisferios, gimnasia cerebral y estilos de aprendizaje
- Educación basada en la evidencia: retos y propuestas de mejora
Alcanzada la escala atómica en la detección magnética
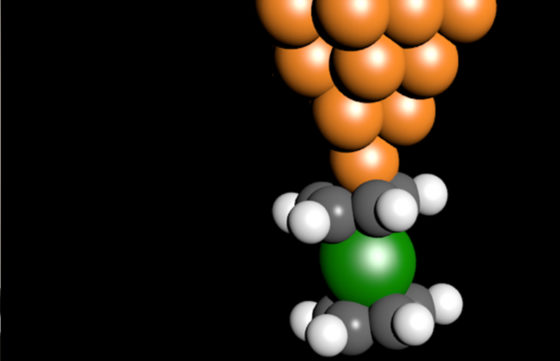
Los resultados, publicados en Science, abren un nuevo camino para obtener información crucial para la comprensión fundamental de las estructuras a escala atómica y para el diseño de futuros dispositivos a escala atómica así como de almacenamiento a nanoescala, o simuladores cuánticos entre otros. Nicolás Lorente, investigador del Centro de Física de Materiales (CFM, centro mixto UPV/EHU–CSIC) y del Donostia International Physics Center (DIPC), y Roberto Robles, también del CFM, son parte del equipo internacional que ha llevado a cabo el trabajo, junto a miembros de las Universidades de Estrasburgo (Francia), y Jülich (Alemania).
Los clásicos microscopios ópticos que utilizan un rayo de luz o de electrones son ciegos e inútiles en la exploración del mundo de los átomos y de las moléculas individuales. En su lugar, se utilizan otras técnicas que pueden ser vistas como una versión diminuta y ultraprecisa de un tocadiscos. Estos instrumentos llamados microscopios de sonda de barrido utilizan el extremo de una aguja afilada como punta para «leer» los surcos creados por los átomos y las moléculas en la superficie de apoyo.
“Para sentir la proximidad entre la punta y la superficie, los científicos utilizamos una pequeña corriente eléctrica que comienza a fluir cuando ambas están separadas por una fracción de millones de milímetros, es decir, un nanómetro. La regulación de la punta para mantener esta distancia permite la obtención de imágenes topográficas mediante el escaneado de la superficie” comenta el Dr. Lorente.
Mientras que los principios básicos de tales microscopios se desarrollaron ya en 1980, solo durante la última década la comunidad científica ha aprendido a ampliar las capacidades de estos microscopios elaborando diseños inteligentes del extremo de su punta de sondeo. Por ejemplo, uniendo una pequeña molécula, como el monóxido de carbono (CO) o el hidrógeno (H2), se logra un aumento sin precedentes en la resolución espacial, en el que la flexibilidad de la molécula hace visibles incluso los enlaces químicos.
De manera similar, los autores de la reciente publicación en Science, presentan un diseño de la afilada punta que aporta una función novedosa: la hace sensible a los momentos magnéticos. Esto se consigue mediante la colocación de un imán molecular que contiene un único átomo de níquel en el ápice. Esta molécula puede ser llevada eléctricamente a diferentes estados magnéticos que tienen en cuenta la dirección en la que señala el imán molecular. La dirección del imán se puede determinar midiendo la conductancia electrónica en el microscopio. Al modo de una pequeña brújula, la punta molecular reaccionará a la presencia de pequeños campos magnéticos en la superficie medida, cambiando la conductancia del microscopio.
“Es la magnitud del dipolo magnético (del imán) de forma que si los dos dipolos se miran con sus lados norte, se repelen con una fuerza proporcional al producto de los momentos magnéticos, y si se miran con polos opuestos se atraen con la misma magnitud”
La importancia de este logro es triple. En primer lugar, el uso de una molécula como sensor activo hace que sea muy reproducible y fácil de implementar en instrumentos utilizados por otros grupos de todo el mundo que trabajan en este campo. En segundo lugar, la técnica no es destructiva ya que las interacciones son muy débiles. En tercer lugar, el esquema de detección se basa únicamente en propiedades fácilmente observables en la punta del sensor de forma que pequeñísimos imanes atómicos que normalmente son difíciles de medir, se vuelven accesibles.
Con este trabajo los científicos han ampliado su caja de herramientas a nanoescala con una nueva técnica sensible a las propiedades magnéticas que será importante para futuras aplicaciones que van desde dispositivos de memoria a nanoescala hasta nuevos materiales o aplicaciones en el campo de la simulación cuántica y la computación.
Referencia:
B. Verlhac, N. Bachellier, L. Garnier, M. Ormaza, P. Abufager, R. Robles, M.-L. Bocquet, M. Ternes, N. Lorente, L. Limot (2019) Atomic-scale spin sensing with a single molecule at the apex of a scanning tunneling microscope Science doi: 10.1126/science.aax8222
El artículo Alcanzada la escala atómica en la detección magnética se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- La óptica se hace atómica: la lente más pequeña del mundo
- Construcción de heteroestructuras de grafeno con precisión atómica
- Biomarcadores para la detección precoz del melanoma
A más datos, mejor servicio público
 Foto: Jacek Dylag / Unsplash
Foto: Jacek Dylag / UnsplashLa digitalización es un aspecto imparable de nuestras sociedades modernas. Cada vez más datos personales acaban en manos de grandes empresas tecnológicas que, en contraprestación, nos ofrecen cada vez nuevos y mejores servicios. Esto, no obstante, conlleva unos riesgos para la privacidad y una preocupación creciente de la ciudadanía, que ya ha visto saltar a los medios diversos escándalos por una gestión poco ética, o directamente ilegal, de esos datos. Leyes como la nueva GDPR europea responden a esa preocupación, y tratan de asegurar que la explotación de nuestros datos se realice con las máximas garantías, aunque todavía queda mucho por hacer.
Recientemente, saltaba la polémica ante la noticia de que diversos organismos públicos, como el INE o el Ministerio de Fomento, están llevando a cabo proyectos para estudiar la viabilidad de obtener un beneficio público de datos procedentes de operadoras de telefonía, ya sea subcontratando estudios o mediante la compra de datos anónimos. En este caso, se trataba de una alarma injustificada provocada por titulares de medios más preocupados por las visitas que por el interés de la ciudadanía. Efectivamente, como muestran muchos estudios científicos, existe un enorme potencial para que la explotación de estos y otros datos mejore la función pública al mismo tiempo que reduzca los costes. Pero además, estos recientes estudios se llevan a cabo con las máximas garantías para preservar nuestro derecho a la privacidad.
El caso del Censo
Un censo es un procedimiento sistemático para adquirir información de una población. Antiguamente, el objetivo era exclusivamente contar a la población. Hoy en día, el registro del Padrón tiene un recuento permanentemente actualizado, y el objetivo de los censos es el de conocer las características de esa población. Se trata de una herramienta de gran tradición (se remonta al siglo XVIII) que aporta una información estadística fundamental para fines no solo gubernamentales, de planificación económica y social, sino también para el tejido empresarial y económico de los países. Tanto es así que su realización es obligatoria por normativa comunitaria, y el ciudadano tiene la obligación por ley de aportar información veraz cuando es encuestado.
En España, el Instituto Nacional de Estadística (INE) es el organismo público encargado de los Censos de Población y Viviendas, que se realizan cada 10 años. La última edición, de 2011, incorporaba una novedad con respecto a la anterior, de 2001: se realizaron encuestas a una muestra representativa (el 10% de la población, unos 4 millones de personas), en lugar de enviar cuestionarios a todas las viviendas del país. Se partía de muy pocos datos por habitante empadronado (tan solo cuatro variables administrativas), y se ideó un procedimiento para inferir todos los demás datos (sociales, familiares, económicos) a partir de la encuesta a esta muestra. Como resultará evidente, se trata de un procedimiento muy complejo y muy costoso.
Los nuevos Censos 2021, en cambio, vendrán cargados de novedades dirigidas a mejorar estas estadísticas y la eficiencia con la que se compilan. El objetivo principal del INE desde 2014, cuando se finalizaron los trabajos de los Censos 2011, es el de aumentar las variables de partida (el INE estima que llegarán hasta el 90%) para disminuir el número de preguntas de la encuesta, haciéndole la vida más fácil al ciudadano, reduciendo el trabajo de procesar todos esos cuestionarios y aumentando la calidad de la información recopilada. Para ello, no solo se cuenta en la actualidad con muchos más registros administrativos (tributarios, seguridad social), aparte del Padrón, sino que se estudia la viabilidad de conseguir parte de esas variables mediante el análisis de datos en manos de compañías privadas.
En concreto, recientemente se ha materializado un acuerdo pionero en Europa entre el INE y tres de las mayores operadoras de telefonía en España. En próximas fechas, se realizará un estudio piloto en el que estas operadoras reportarán al INE recuentos de la presencia de teléfonos móviles para ciertas franjas horarias en una serie de “áreas INE” en las que han dividido el país. Estas áreas se han definido bajo el criterio de que contengan un mínimo de 5000 habitantes para ofrecer las máximas garantías en cuanto a anonimidad de los datos, y el INE ha desarrollado una metodología para su aprovechamiento con tres objetivos fundamentales: obtener 1) dónde vive la población, 2) adónde se mueve diariamente (principalmente por motivos de trabajo), y 3) con qué otras zonas está vinculada (por ejemplo, viaje al pueblo en Navidad). Los dos últimos objetivos están relacionadas con dos preguntas referentes a movilidad que ya estaban presentes en los dos últimos censos, mientras que el primero es una estimación complementaria de la población que servirá para cuantificar y corregir posibles sesgos.
El caso de la movilidad
Otro aspecto tanto o más importante para las políticas públicas que las características de la población es cómo nos movemos. Muchos investigadores estamos convencidos de que la cantidad masiva de datos que generamos con nuestra actividad diaria puede analizarse de forma ética para obtener grandes beneficios sociales en este aspecto. No en vano, la mayor parte del conocimiento que tenemos de nuestras ciudades se basa en estos censos que se realizan cada 10 años y contienen información estática. Investigaciones como el Atlas de la Desigualdad, del profesor Esteban Moro (Universidad Carlos III de Madrid, profesor visitante en el MIT Media Lab), tratan de ir un paso más allá y combinar la información censal con datos de geoposicionamiento para tener una visión más granular de los problemas de las ciudades modernas.
El Ministerio de Fomento también empieza a ser consciente del potencial de este tipo de datos en beneficio de todos, y en concreto para estudiar la movilidad de los ciudadanos y planificar las infraestructuras y sistemas de transportes. Al igual que con el censo, hasta ahora la fuente principal de información también eran encuestas. La última gran encuesta, Movilia 2006/2007, nos costó 5 millones de euros. Sin embargo, en 2018 se contrató un estudio con objetivos similares a partir de datos telefónicos, cuyo coste fue de tan solo 150 mil euros, aunque todavía no son públicos sus resultados.
Datos para el bien social
Toda esta información estadística es un bien público necesario para el buen funcionamiento de un país, para el diseño, evaluación y mejora de las políticas públicas. La empresa privada ya hace tiempo que se subió al carro de la digitalización, y hace cada vez un mayor uso de la ciencia de datos para optimizar sus procesos internos y tomar decisiones basadas en datos, para crecer y aumentar su competitividad en el mercado. Es el momento de que la administración pública tome el mismo camino y se modernice en beneficio de todos.
Como ciudadanos, no solo deberíamos alegrarnos de que por fin se tomen estas iniciativas, sino que deberíamos exigir activamente que nuestros datos se usen para el bien social; eso sí: siempre con las máximas garantías y transparencia, de forma ética y respetuosa con nuestro derecho a la privacidad. Es el momento de exigir políticas y una gestión basadas en datos.
Sobre el autor: Iñaki Úcar es doctor en telemática por la Universidad Carlos III de Madrid e investigador postdoctoral del UC3M-Santander Big Data Institute.
El artículo A más datos, mejor servicio público se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Datos que entran por los ojos
- Los orígenes de la visualización de datos
- Humildemente, el mundo es mejor gracias a mí
El puzzle Stomachion y el palimpsesto de Arquímedes (2)
En la primera entrada de esta mini-serie de la sección Matemoción del Cuaderno de Cultura Científica, El puzzle Stomachion y el palimpsesto de Arquímedes (1), habíamos descrito el rompecabezas conocido como Stomachion, o caja de Arquímedes, e incluso analizado las áreas de las piezas que lo componen, pero, sobre todo, habíamos contado la sorprendente historia del palimpsesto de Arquímedes, que incluye la copia más extensa de la obra Stomachion del gran matemático griego Arquímedes de Siracusa (aprox. 287 – 212 a.n.e.). Por otra parte, en la presente entrada vamos a centrarnos en algunos aspectos matemáticos del Stomachion.
 Rompecabezas Stomachion, también llamado Ostomachio o caja de Arquímedes
Rompecabezas Stomachion, también llamado Ostomachio o caja de Arquímedes
Empecemos recordando que el Stomachion es un rompecabezas de tipo Tangram formado por 14 piezas, en concreto, 11 triángulos, 2 cuadriláteros y 1 pentágono, que podemos ver en la imagen anterior.
Si consideramos que el cuadrado generador tiene unas dimensiones de 12 unidades de longitud (por ejemplo, centímetros) de lado y trazamos la cuadrícula 12 x 12 sobre el mismo, como hicimos en la entrada anterior, se puede observar que todos los vértices de las piezas descansan sobre los puntos de intersección de la cuadrícula. Notemos además que, en la cuadrícula, la distancia entre un punto de la misma y el siguiente, en horizontal o vertical, es una unidad de longitud. Esto, además de dejar claro que esta descomposición del cuadrado no es caprichosa, nos permite calcular fácilmente las áreas de las 14 piezas del rompecabezas, todas con valores enteros (desde arriba a la izquierda, siguiendo el orden de las agujas del reloj, más o menos): 12, 6, 12, 24, 3, 9, 6, 12, 6, 21, 3, 6, 12 y 12.
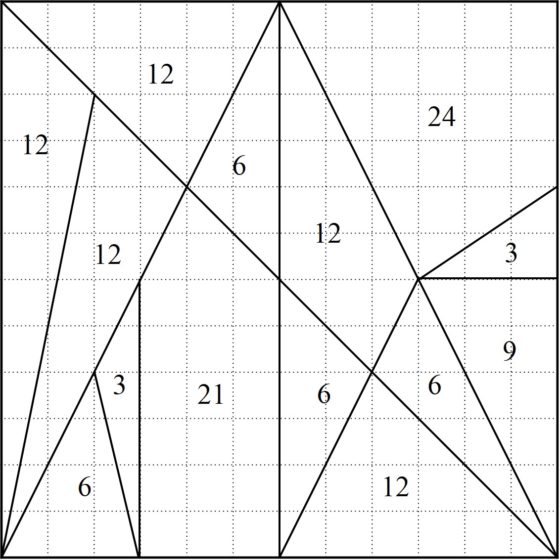 Áreas de las 14 piezas del puzle de Arquímedes, Stomachion
Áreas de las 14 piezas del puzle de Arquímedes, Stomachion
El cálculo de las áreas es sencillo y puede ser un interesante problema para el aula de matemáticas, pero aún le podemos sacar un poco más de partido al tema de las superficies, comprobando que los anteriores resultados son correctos mediante el teorema de Pick, como nos sugiere el grupo Alquerque de Sevilla en su artículo sobre el Stomachion en la revista Suma.
Teorema de Pick (1899): si un polinomio P tiene sus vértices sobre una cuadrícula, entonces su área es igual a
![]()
donde B es un número de puntos de la cuadrícula que están en el borde del polígono e I los que están en el interior del mismo.
En la siguiente imagen podemos ver la comprobación del teorema de Pick para las piezas verde y azul. Hemos pintado los puntos del borde de los polígonos (cuyo número es B) de amarillo y los del interior de verde (cuyo número es I).
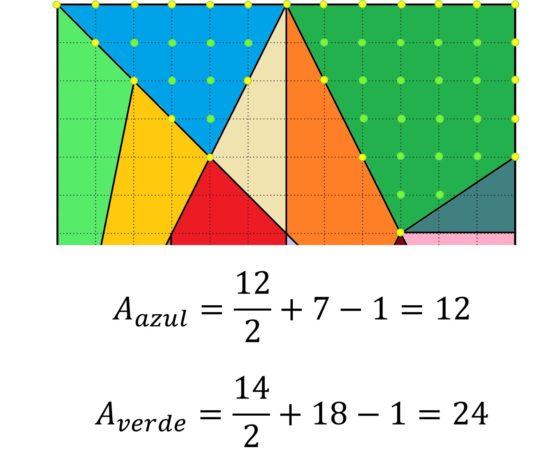 El teorema de Pick aplicado al cálculo de las áreas de las piezas verde y azul del Stomachion
El teorema de Pick aplicado al cálculo de las áreas de las piezas verde y azul del Stomachion
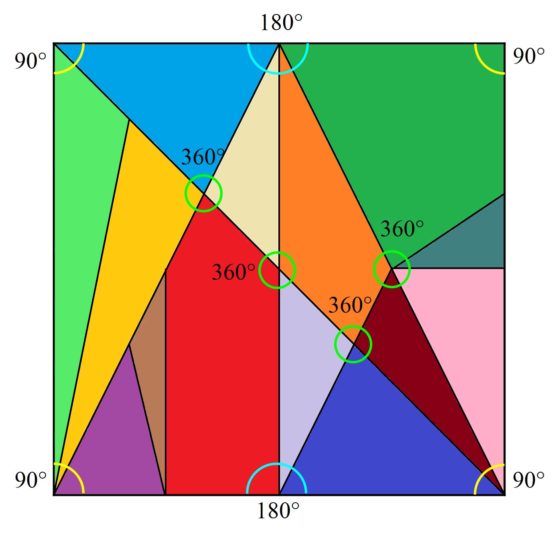
A continuación, vamos a analizar los ángulos de las piezas de la caja de Arquímedes. Esta es una cuestión importante también, puesto que cuando se trabaja la resolución de puzzles geométricos como el Tangram, los rompecabezas de letras, como T y M, u otros similares, el razonamiento sobre los ángulos es fundamental para la resolución de los mismos. Por ejemplo, en estos puzzles cuadrados, en las esquinas debe ir una pieza rectangular o la suma de los ángulos de las piezas que tocan la esquina debe ser 90º, los ángulos en los vértices que están en los lados del cuadrado deben sumar 180º, mientras que en los vértices interiores deben sumar 360º (véase en la imagen algunos ejemplos).
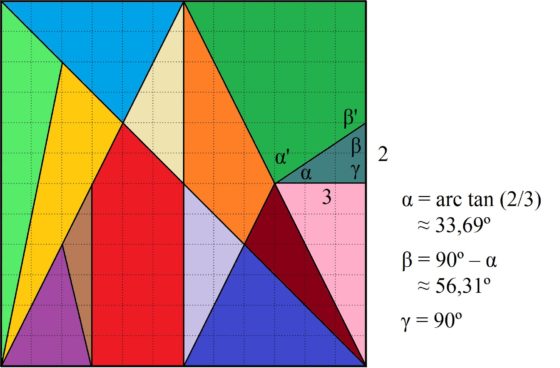
Para empezar, fijémonos en la pieza que es un triángulo rectángulo, de área 3 en la cuadrícula 12 x 12, que está en la parte derecha de la imagen anterior del puzzle (de color azul grisáceo en la imagen coloreada). Si estudiamos los ángulos de esta figura, uno es 90º (ángulo recto), pero los otros son alpha = arctan (2/3) = 33,69º (aprox.) y beta = 90º – alpha = 90º – 33,69º = 56,31º (aprox.). Como veremos más adelante, la mayoría de los ángulos de las piezas del Stomachion están relacionados con el ángulo delta = arctan (1/2) = 26,57º (aprox.) y los ángulos alpha y beta de este pequeño triángulo rectángulo solo encajan con los ángulos alpha’ y beta’ de la pieza que es un cuadrilátero con un ángulo recto (la pieza verde oscuro en la imagen coloreada). Como consecuencia de esto las dos piezas anteriores, el cuadrilátero con un ángulo recto y el pequeño triángulo rectángulo, siempre irán juntas en cualquier solución del juego original, es decir, colocar las piezas del rompecabezas para montar un cuadrado.
Un análisis similar puede realizarse con las piezas verde claro y naranja, que irán juntas en cualquier solución de la caja de Arquímedes. Y lo mismo las piezas morada y marrón. Por este motivo, en los análisis matemáticos de este juego geométrico se suele juntar cada una de estas parejas de piezas para formar una pieza común. De hecho, la matemática estadounidense nacida en Taiwán Fan Chung y el matemático estadounidense Ron Graham llaman a este nuevo puzzle el Stomach (le han quitado tres letras al nombre, al igual que el nuevo rompecabezas ahora tiene tres piezas menos), y veremos más adelante el análisis que hacen del mismo.
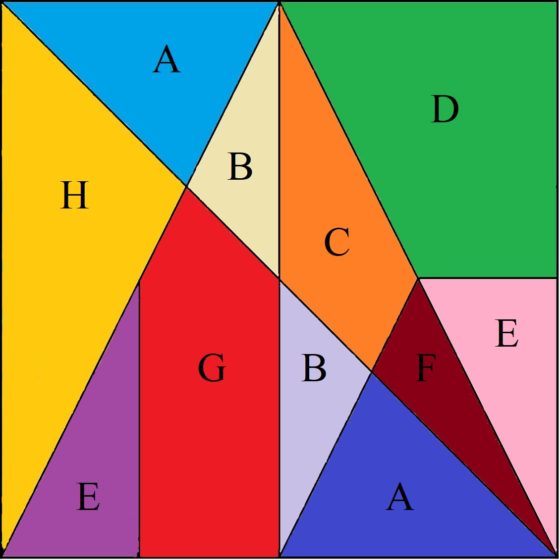 Rompecabezas Stomach, formado por 11 piezas, 8 triángulos, dos cuadriláteros y un pentágono. Las piezas han sido nombradas con una letra, de forma que las piezas que tienen la misma forma tengan la misma letra, como ocurre con A, B y E
Rompecabezas Stomach, formado por 11 piezas, 8 triángulos, dos cuadriláteros y un pentágono. Las piezas han sido nombradas con una letra, de forma que las piezas que tienen la misma forma tengan la misma letra, como ocurre con A, B y E
Ahora, de nuevo con un poco de trigonometría básica (de hecho, basta la definición geométrica de la tangente de un ángulo y que la suma de los ángulos de un triángulo es 180º) se pueden calcular los ángulos de las piezas del Stomach (en general, del Stomachion), que como hemos comentado están la mayoría expresados en función del ángulo delta = arctan (1/2) = 26,57º (en la imagen siguiente puede verse, por ejemplo, en el triángulo rosa que el ángulo delta es aquel cuya tangente vale 3/6 = 1/2).
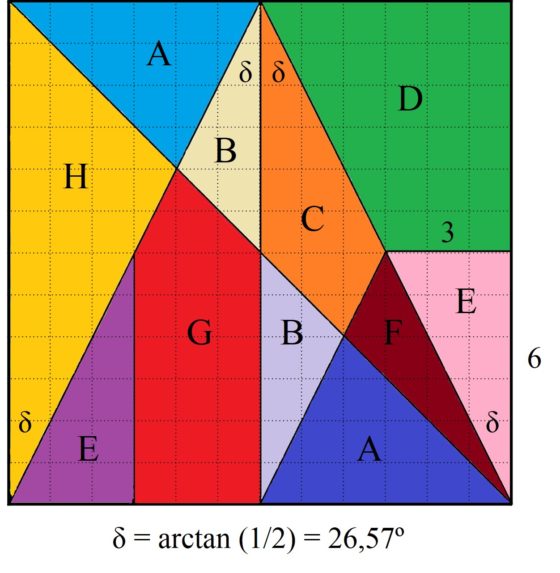
A continuación, mostramos en una tabla los valores de los ángulos de las piezas del Stomach (que son las del Stomachion, con la salvedad de las tres uniones que hemos realizado). Empezamos por las piezas de arriba a la derecha, desde la pieza A, y enumeramos los ángulos desde la derecha y en el sentido de las agujas del reloj.
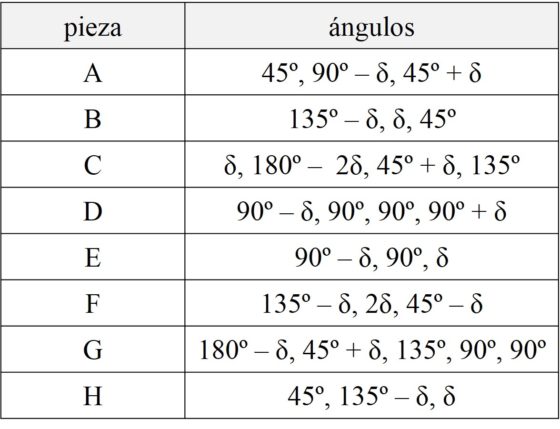
Pero volvamos a la obra Stomachion de Arquímedes, dedicada al rompecabezas homónimo. Como comentamos en la anterior entrada El puzzle Stomachion y el palimpsesto de Arquímedes (1), el mayor fragmento conservado de esta obra, aunque es solamente una página y además la parte introductoria de la misma, apareció en el palimpsesto de Arquímedes. Esta obra despistó completamente a los expertos, ya que aparentemente trataba sobre un juego infantil sin ningún interés científico, lo cual no se correspondía con la profundidad científica de sus demás obras.
El historiador de las matemáticas israelí Reviel Netz, profesor de la Universidad de Stanford en California, después de investigar el Stomachion concluyó que, en su opinión, no era simplemente una sencilla obra sobre un juego infantil, sino que se trataba realmente de un tratado de combinatoria.
La combinatoria es una rama de las matemáticas, que entre otras cuestiones incluye el estudio de métodos para contar las estructuras o configuraciones de un conjunto de un determinado tipo o tamaño. Por ejemplo, son problemas de la combinatoria el contar cuántos cuadrados latinos existen de un orden dado (véase la entrada Cuadrados latinos, arte y matemáticas), cuántas soluciones tiene una ecuación lineal (véase Aprendiendo técnicas de contar: lotería primitiva y bombones), cómo se pueden distribuir una serie de elementos con unas ciertas condiciones (véase El problema matemático de las cartas extraviadas o El problema de las estudiantes de Kirkman), o cuántas soluciones tiene un juego o puzzle (véase Cubo soma: diseño, arte y matemáticas o el libro Del ajedrez a los grafos).
En opinión de Reviel Netz la cuestión que le interesaba a Arquímedes en relación al rompecabezas era cuántas soluciones existen del mismo, es decir, de cuántas formas distintas se pueden colocar las 14 piezas para formar un cuadrado. Mientras que para el Tangram solo hay una manera de construir el cuadrado, es decir, solo existe una solución, más allá de rotaciones (girar el cuadrado), reflexiones (darle la vuelta) o cambiar las piezas de igual forma entre sí, las piezas geométricas del Stomachion se pueden combinar de diferentes formas para dar lugar al cuadrado, esto es, tiene muchas soluciones. Este era el problema combinatorio del tratado de Arquímedes, por lo tanto, de una profundidad mayor de la que aparentaba.
Por lo tanto, el problema combinatorio quedaba abierto, ¿de cuántas formas distintas se puede resolver la caja de Arquímedes? El profesor Netz no sabía cómo de difícil podía ser este problema y si Arquímedes pudo resolverlo en su tratado, por lo que se lo planteó a algunos colegas de su universidad, la profesora de estadística Susan Holmes y el matemático Persi Diaconis, conocido por su trabajo en magia y matemáticas. Como explica la propia Susan Holmes: “al principio pensamos que podíamos sentarnos y resolver en un día cuántas soluciones tenía. Entonces nos dimos cuenta de que eran muchas más de las que podíamos haber imaginado”. Entonces, junto con la pareja de profesores de la Universidad de California, Ron Howard y Fan Chung, dedicaron varios meses a resolver esta cuestión combinatoria. Finalmente, obtuvieron la respuesta buscada, hay 17.152 configuraciones distintas de todas las piezas del Stomachion que forman un cuadrado, que se reducen a 536, si no tenemos en cuenta rotaciones, reflexiones o el intercambio de las piezas que son iguales (las piezas A y B en la imagen del Stomach), 536 x 32 = 17.152.
 Cada solución del Stomachion, como la original de la construcción, da lugar a 8 soluciones mediante rotaciones y reflexiones, como se muestra en la imagen. Además, cada una de estas da lugar, a su vez, a 4 soluciones intercambiando de lugar las piezas de igual forma, A y B. Por este motivo, 536 x 8 x 4 = 17.152 soluciones
Cada solución del Stomachion, como la original de la construcción, da lugar a 8 soluciones mediante rotaciones y reflexiones, como se muestra en la imagen. Además, cada una de estas da lugar, a su vez, a 4 soluciones intercambiando de lugar las piezas de igual forma, A y B. Por este motivo, 536 x 8 x 4 = 17.152 soluciones
Aunque un poco antes, en noviembre de 2003, el informático Guillermo H. Cutler, que había diseñado un programa informático para resolver el problema, encontró las 536 formas distintas de combinar las 14 piezas del rompecabezas para formar el cuadrado.
 536 soluciones del Stomachion obtenidas por Guillermo H. Cutler
536 soluciones del Stomachion obtenidas por Guillermo H. Cutler
Por otra parte, la profesora Chung y el profesor Graham visualizaron las soluciones de la caja de Arquímenes, y las relaciones entre las mismas, a través de un grafo, que vamos a explicar brevemente en lo que queda de entrada. La construcción es delicada, pero de una gran profundidad y belleza.
Para empezar, Fan Chung y Ron Howard no estudiaron directamente las soluciones del Stomachion, sino de un nuevo rompecabezas que llamaron Stomach y que hemos mostrado más arriba. Las soluciones son prácticamente las mismas. De hecho, cada solución del Stomach da lugar a dos soluciones del Stomachion ya que la pieza E rosa, se puede intercambiar con la pieza E morada, la cual está formada por dos piezas del Stomachion original. De hecho, el Stomach tiene 268 configuraciones básicas, que dan lugar a las 268 x 2 = 536 configuraciones básicas del Stomachion.
Para visualizar las soluciones del Stomach, Chung y Howard construyeron un grafo. Recordemos que un grafo está formado simplemente por puntos –llamados vértices del grafo- y líneas que unen algunos de esos puntos –llamadas aristas del grafo- (véase, por ejemplo, El problema de los tres caballeros y los tres criados [https://culturacientifica.com/2016/05/04/problema-los-tres-caballeros-los-tres-criados/], El grafo de Marion (gray) [https://culturacientifica.com/2019/07/31/el-grafo-de-marion-gray/] o El juego de Sim [https://culturacientifica.com/2017/04/19/juego-del-sim/], entre otros), y que es una estructura matemática muy sencilla, pero a la vez muy versátil.
En el grafo introducido por Chung y Howard, asociado al rompecabezas geométrico, cada vértice es una de las configuraciones de las piezas formando el cuadrado, es decir, una de las 268 soluciones del rompecabezas, mientras que dos vértices están unidos por una arista si existe un movimiento, local o global (cuyo significado explicaremos un poco más adelante), que transforma una configuración en otra.
Para empezar, describamos lo que esta pareja de matemáticos denomina “núcleo” del grafo, que está formado por 24 configuraciones particulares y los movimientos entre ellas.
Si se consideran las 11 piezas del Stomach, solo existe una forma de dividirlas en cuatro grupos para formar cuatro triángulos rectángulos básicos, que juntos dan lugar al cuadrado del rompecabezas, que llamaremos triángulos básicos 1, 2, 3, 4, siguiendo la notación de Chung y Howard. Estos triángulos son:
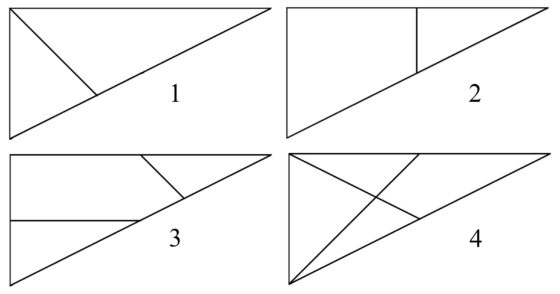
El núcleo del grafo está formado por las 24 soluciones básicas que se obtienen juntando estos cuatro triángulos, tomados tal cual están, salvo que los rotemos, o volteados. La notación que vamos a utilizar es la siguiente. Cada configuración básica estará nombrada por los cuatro números de los cuatro triángulos básicos en el orden que están colocados desde la izquierda a la derecha, y si un triángulo está volteado utilizamos un signo prima para marcarlo. Por ejemplo, la solución inicial del Stomach que está más arriba, coloreada, sería 1’ 2’ 3 4, ya que la pieza 1 está a la izquierda, pero volteada, lo mismo que la siguiente, que es la 2, mientras que luego van, sin voltear, las piezas 3 y 4.
A continuación, mostramos la imagen con las 24 configuraciones del núcleo, con la correspondiente notación.
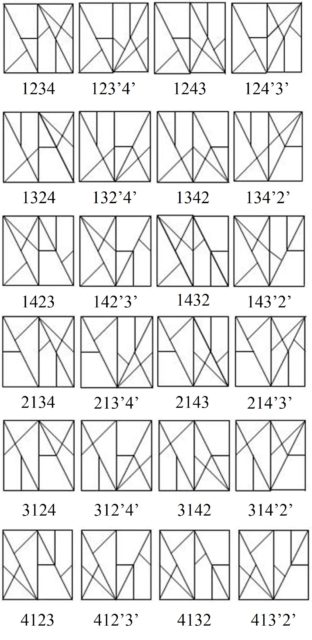
Además, estas configuraciones del núcleo están conectadas por movimientos globales (que van a ser las aristas del grafo) que consisten en intercambiar dos de los cuatro triángulos básicos (la pieza 1 la podemos mantener sin dar la vuelta y siempre en la parte de la izquierda, respecto al centro).
Por ejemplo, la configuración 1234 está conectada, con una arista, a las configuraciones 1324, 1243, 124’3’, 123’4’ y 2134, puesto que se puede llegar a ellas intercambiando dos de los triángulos básicos de 1234, como se ve fácilmente. En teoría de grafos se dice que el vértice 1234 tiene grado 5, ya que hay 5 aristas conectadas con el mismo (por ahora).
Podemos formar ahora la parte de este grafo que es el núcleo, cuyos vértices son las 24 configuraciones anteriores y las aristas están dadas por los movimientos globales que acabamos de describir. El resultado sería el siguiente.
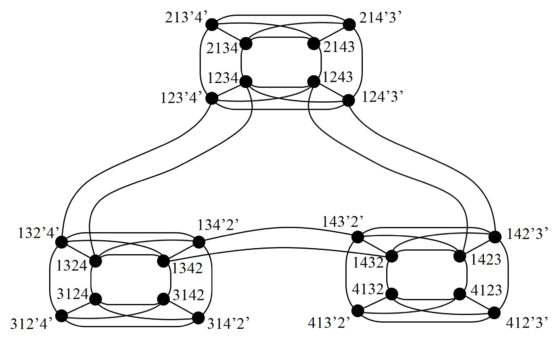
Por otro lado, cada una de esas 24 configuraciones básicas está conectada, mediante aristas que vienen de movimientos locales, con otras configuraciones del cuadrado. Un movimiento local de una configuración consiste en rotar o voltear una subregión simétrica del cuadrado formada por un grupo de piezas contiguas. Por ejemplo, en la imagen de abajo el grupo de piezas formado por los dos triángulos azules, que es un triángulo isósceles, ha sido volteado para dar lugar a otra solución distinta del rompecabezas, otra configuración.
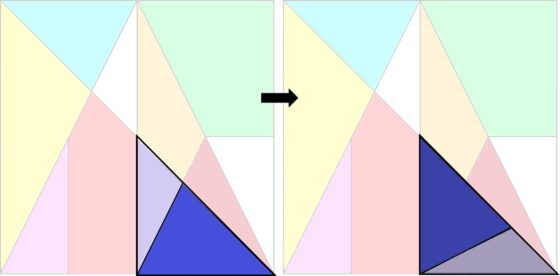
Dada una de las 24 configuraciones básicas, llamémosle B, la estructura de las configuraciones que se pueden alcanzar a partir de ella, mediante movimientos locales, es denominada por Chung y Howard el “cluster” de B. En la siguiente imagen vemos el cluster de la configuración básica 1234, con el grafo asociado al mismo, que es un grafo con 7 vértices/representaciones (podéis descubrir en la imagen el movimiento local que se produce entre una configuración y otra conectada). Notemos que se han coloreado los vértices en función de la distancia a la configuración básica del núcleo (cada arista recorrida aumenta una unidad la distancia), en este ejemplo, la distancia a 1234.
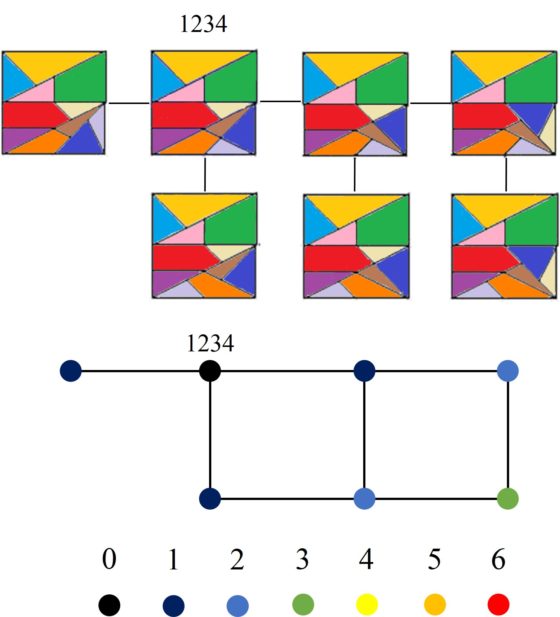
Los clusters de las configuraciones básicas no son siempre iguales. Por ejemplo, el cluster de la configuración 1324 tiene diez vértices, como vemos en la siguiente imagen.
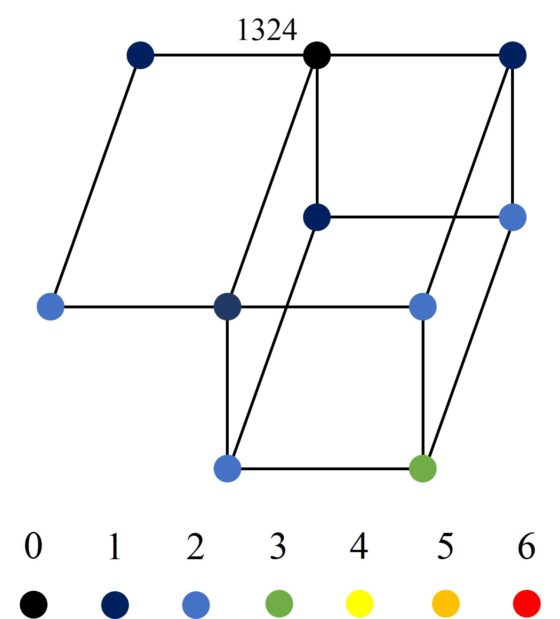
Además, la arista entre dos vértices del núcleo, es decir, entre dos configuraciones básicas, se extiende a aristas entre los vértices de sus clusters. Si los clusters tienen la misma estructura, como los de los vértices 1234 y 2134, las aristas se extienden de forma paralela, como se ve en la siguiente imagen.
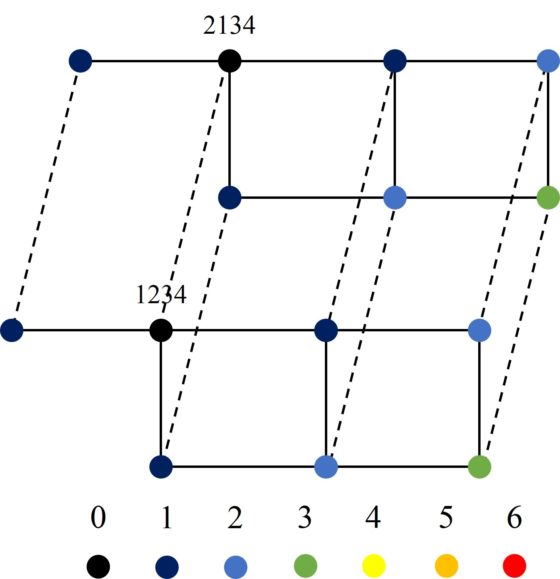
Mientras que, si los clusters tienen distintas estructuras, entonces las aristas que unen vértices de los dos clusters son más particulares, como entre los vértices 1234 y 1324.
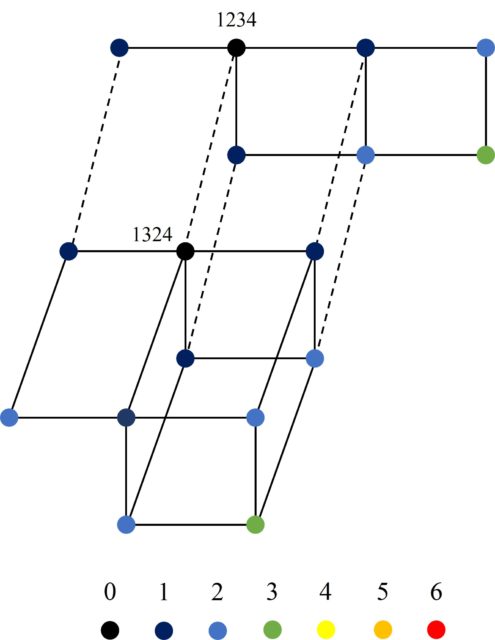
Existen seis estructuras diferentes de clusters, aunque la mayoría de las configuraciones básicas están relacionadas con tres de ellos. La estructura del cluster de las ocho configuraciones básicas que están en la parte superior de la imagen del grafo del núcleo (1234, 1243, 2143, 2134, 213’4’, 123’4’, 124’3’, 214’3’) es la misma. La llamaremos “estructura de cluster A” y tiene 7 vértices. También comparten estructura de cluster seis de las ocho configuraciones básicas que están en la parte izquierda de la imagen del grafo del núcleo (1324, 3124, 3142, 132’4’, 312’4’, 314’2’). La llamaremos “estructura de cluster B” y tiene 10 vértices. Y la otra estructura de cluster repetida, que llamaremos “estructura de cluster C”, tiene 14 vértices y es compartida por 7 de las ocho configuraciones básicas que están en la parte derecha de la imagen del grafo del núcleo (1423, 4123, 4132, 143’2’, 142’3’, 412’3’, 413’2’). Estas tres estructuras de clusters son las que aparecen en la siguiente imagen.
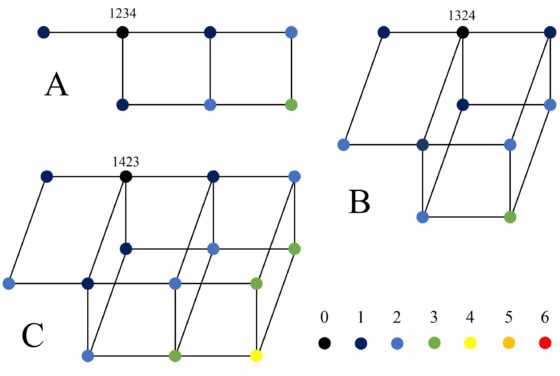
Mientras que hay tres configuraciones básicas, cada una de las cuales tiene su propia estructura particular de cluster. La configuración 1432 tiene la siguiente estructura de cluster, que llamaremos D, con 18 vértices.
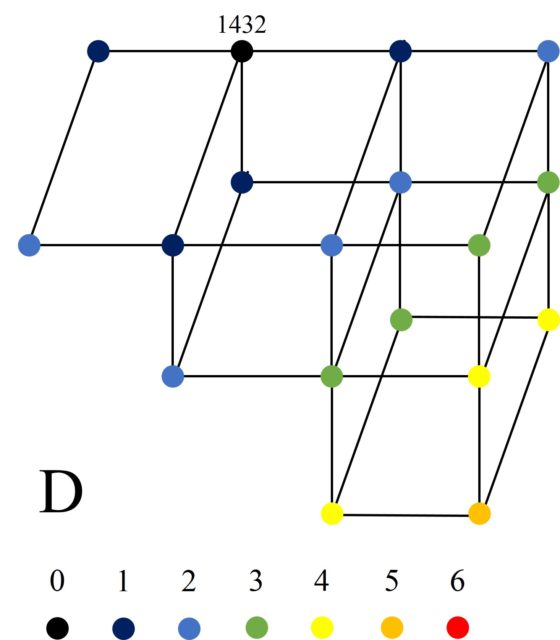
La configuración 1342 tiene la estructura de cluster que llamaremos E, con 16 vértices.
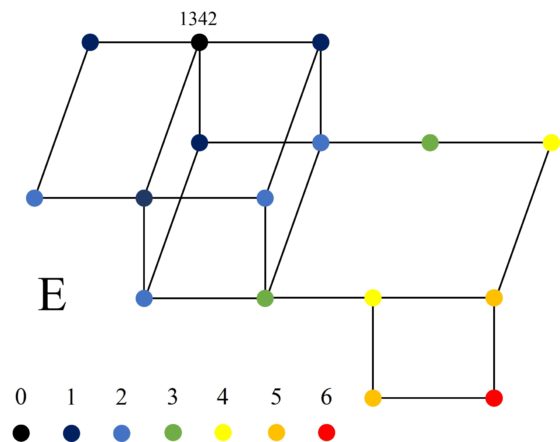
Y la configuración 134’2’ tiene la estructura de cluster más raras de todas, también con 18 vértices, que llamaremos F.
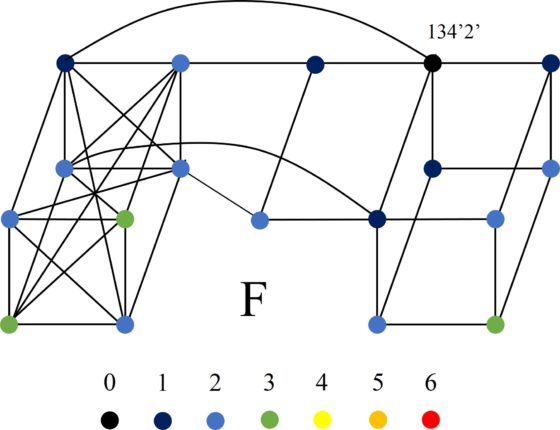
En resumen, el grafo gigante que hemos generado con soluciones/configuraciones del Stomach posee 266 vértices (que recordemos que son las soluciones del rompecabezas geométrico) y 936 aristas (que recordemos que están generadas a partir de movimientos locales y globales sobre las soluciones del Stomach). Pero resulta que hemos generado un grafo (conexo, es decir, no hay grupos de vértices desconectados, mediante las aristas, del resto) con 266 vértices, pero recordemos que el número de soluciones básicas del Stomach son 268. ¿Qué ocurre con las otras dos soluciones/configuraciones del puzzle? Resulta que esas dos configuraciones, están conectadas entre ellas mediante un movimiento local, es decir, son dos vértices con una arista entre ellas, pero están desconectadas del resto de soluciones del rompecabezas. Estas configuraciones son las que aparecen en la imagen siguiente.
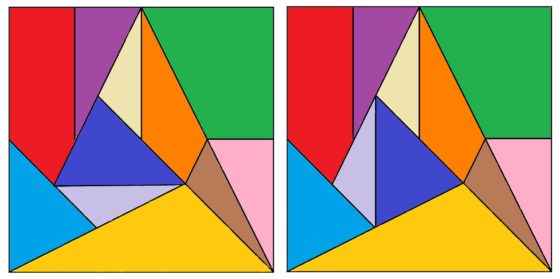
En la siguiente imagen, para comprender un poco mejor la estructura de este enorme grafo asociado con el puzzle geométrico Stomach, hemos vuelto a dibujar el núcleo, indicando en cada configuración básica cual es la estructura de cluster que se agrega a la misma, así como las dos configuraciones aisladas, que no están en el núcleo o conectadas con el mismo, que hemos denominado “configuración 267” y “configuración 268”.
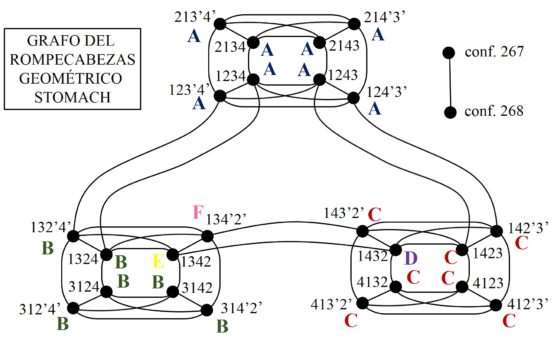
Todos los detalles de esta construcción, incluidas las aristas entre clusters de diferente estructura que no hemos incluido aquí, pueden encontrarse en la página A tour of Archimedes’ Stomachion, de la matemática Fan Chung y el matemático Ron Graham. Además, se incluyen interesantes propiedades matemáticas del grafo, como las dos con las que concluimos esta entrada.
Si consideramos la componente más grande del grafo del Stomach, con 266 vértices y 936 aristas, esta tiene un diámetro de 11, es decir, la distancia más grande entre dos vértices del grafo es de 11 aristas. Además, este subgrafo es un grafo de los llamados hamiltonianos, es decir, existe un camino (sucesión de vértices y aristas) que pasa por todos los vértices y en el que no se repite ningún vértice. Uno de esos caminos se muestra en la página A tour of Archimedes’ Stomachion, para quien esté interesado.
Y, para terminar, una escultura relacionada con los caminos hamiltonianos.
 Escultura Hamilton cycle on football, del matemático y artista holandés Koos Verhoeff, en el exterior del edificio de Matemáticas de la Universidad de Heidelberg
Escultura Hamilton cycle on football, del matemático y artista holandés Koos Verhoeff, en el exterior del edificio de Matemáticas de la Universidad de Heidelberg
Bibliografía
1.- Reviel Netz, Fabio Acerbi, Nigel Wilson, Towards a Reconstruction of Archimedes’ Stomachion, SCIAMV 5, pp. 67-99, 2004.
2.- Grupo Alquerque de Sevilla (Juan Antonio Hans, José Muñoz, Antonio Fernández-Aliseda), Stomachion, el cuadrado de Arquímedes, SUMA, n. 50, pp. 79 – 84, 2005.
3.- Fan Chung, Ron Graham, A tour of Archimedes’ Stomachion
4.- Raúl Ibáñez, Del ajedrez a los grafos, la seriedad matemática de los juegos, colección El mundo es matemático, RBA, 2015.
5.- Erica Klarreich, Glimpses of genius, Science News, n. 15, vol. 165, 2004.
6.- Wolfram Mathworld: Stomachion
7.- Tom Verhoeff, Koos Verhoeff, Three Mathematical Sculptures for the Mathematikon, Proceedings of Bridges 2016: Mathematics, Music, Art, Architecture, Education, Culture, pp. 105-110, 2016.
Sobre el autor: Raúl Ibáñez es profesor del Departamento de Matemáticas de la UPV/EHU y colaborador de la Cátedra de Cultura Científica
El artículo El puzzle Stomachion y el palimpsesto de Arquímedes (2) se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- El puzzle Stomachion y el palimpsesto de Arquímedes (1)
- Un delicioso puzzle de chocolate
- Un puzzle sencillo
El modelo de Bohr explica las regularidades en el espectro del hidrógeno
 Foto: Tyler Lastovich / Unsplash
Foto: Tyler Lastovich / UnsplashCuando Bohr propuso su modelo en 1913, solo se conocían las líneas de emisión del hidrógeno en las series Balmer y Paschen. Balmer había sugerido, y el modelo de Bohr concordaba con ello, que deberían existir series adicionales.
Experimentos contemporáneos y posteriores descubrieron la serie de Lyman en la porción ultravioleta del espectro (1904–1914), la serie de Brackett (1922) y la serie de Pfund (1924), estando estas últimas en la región infrarroja del espectro. En cada serie se encontró que las frecuencias medidas de cada una de las líneas eran las predichas por el modelo de Bohr y, lo que es más importante, no aparecían líneas que no se correspondiesen con el modelo. Del mismo modo, el modelo de Bohr podía explicar la fórmula general que Balmer supuso que podría aplicarse a todas las líneas espectrales de hidrógeno. Descritas términos empíricos, las líneas de la serie de Lyman corresponden a transiciones de varios estados iniciales al estado final nf =1; las líneas de la serie Paschen corresponden a transiciones de varios estados iniciales al estado final nf = 3; y así sucesivamente, como lo indica la expresión derivada a partir del modelo de Bohr:
1/λ = RH (1/nf2 – 1/ni2)
El esquema general de posibles transiciones entre las primeras seis órbitas se muestra en la figura 1.
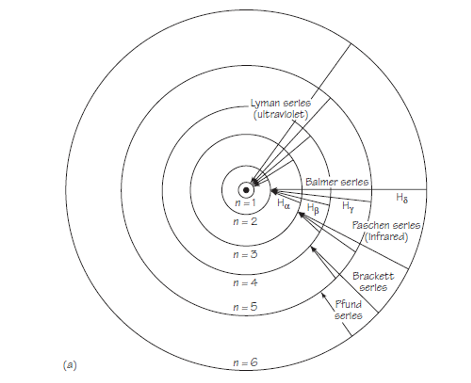 Fuente: Cassidy Physics Library
Fuente: Cassidy Physics LibraryPor lo tanto, el modelo no solo relacionó información conocida sobre el espectro de hidrógeno, sino que también predijo correctamente las longitudes de onda de series de líneas previamente desconocidas en el espectro. Además, proporcionó un modelo físico razonable; la fórmula general de Balmer no había proporcionado ninguna razón física para la relación empírica entre las líneas de cada serie.
El diagrama de la figura 1 es útil como ayuda para la imaginación. Pero tiene el peligro de ser demasiado específico. Por ejemplo, puede llevar a pensar en la emisión de radiación como «saltos» reales de electrones entre órbitas. [*]
Existe otra forma de presentar los resultados de la teoría de Bohr que produce los mismos resultados pero no se adhiere tan estrechamente a una imagen de órbitas. Este nuevo esquema se muestra en la figura 2. No se centra en las órbitas sino en los estados de energía posibles correspondientes. Todos estos estados de energía vienen dados por la expresión para la energía del estado estacionario, En = 1/n2 ·E1 .
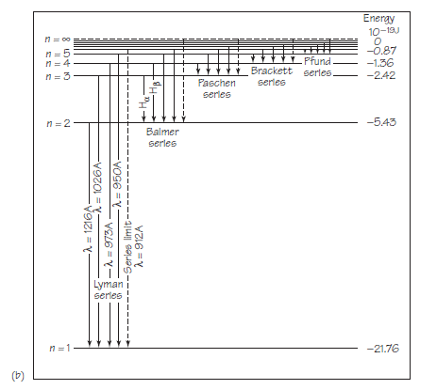 Fuente: Cassidy Physics Library
Fuente: Cassidy Physics LibraryEn términos de este modelo matemático, el átomo normalmente no está excitado, con una energía E1 de aproximadamente 13,6 eV (o 22 1019 J). La absorción de energía puede colocar a los átomos en un estado excitado, con una energía correspondientemente más alta. El átomo excitado está entonces listo para emitir radiación, con la consiguiente reducción de energía. La energía absorbida o emitida siempre cambia la energía total del átomo a uno de los valores especificados por la fórmula para En. Por lo tanto, el átomo de hidrógeno también puede representarse, no por órbitas, sino por medio de un diagrama de niveles de energía.
Nota:
[*] Es necesario profundizar un poco más en la cuántica para comprender que esto no es posible, porque no podemos, de entrada, localizar un electrón. Lo veremos en una próxima serie.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
El artículo El modelo de Bohr explica las regularidades en el espectro del hidrógeno se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- El modelo de Bohr explica la fórmula de Balmer
- Las regularidades en el espectro del hidrógeno
- El tamaño del átomo de hidrógeno
Desmitificando: Vacunas peligrosas
 Imagen de Ria Sopala / Pixabay
Imagen de Ria Sopala / PixabayLos datos son de Estados Unidos. Antes de las vacunas algo más de 21000 personas tuvieron difteria; en la era de las vacunas, el número bajó a cero. Para la varicela, el porcentaje de caída del número de enfermos fue del 89%. Para la polio, el 100%, la viruela, el 100%; el tétanos, el 98%. Y así podemos seguir, enfermedad tras enfermedad. Los males que ahora padece nuestra especie, en general, son aquellos para los que no hay vacuna, y, en cambio, muchos con vacuna han sido prácticamente erradicados. Males que diezmaban generaciones hace no muchos años. La OMS, en 2018, resume que las vacunas protegen al 86% de la población mundial, y evitan la muerte de dos millones de personas cada año.
En 1980 se declaró desaparecida la viruela y, ahora, se debate si hay que destruir los pocos cultivos de virus de la viruela que se conservan en algunos laboratorios de alta seguridad. En 2016 solo se registraron 42 casos de polio en todo el mundo y todos ellos en cuatro países: Pakistán, Afganistán, Laos y Nigeria. La enfermedad infectó a unas pocas personas por razones religiosas y sociales, no por causas médicas. Fue en la década de los cincuenta del siglo pasado cuando, primero Jonas Salk y, poco después, Albert Sabin, desarrollaron vacunas contra la polio. Ahora, 60 años después, la vacuna ha eliminado la enfermedad de casi todo el planeta. Jonas Salk renunció a la patente de su vacuna y proclamó que “no se puede patentar el sol”.
Vista la historia de las vacunas, parece que la confianza en ellas debía ser total. Sin embargo, la confianza en su eficacia se ha convertido en un asunto de salud pública global de importancia creciente. La caída en la confianza en las vacunas lleva a la vuelta de enfermedades casi olvidadas y casi erradicadas o a impedir que otras desaparezcan, como ocurre con la polio o las paperas, y a múltiples debates sociales y políticos en muchos países, sean ricos o en desarrollo. El grupo de Heidi Larson, de la Escuela de Higiene y Medicina Tropical de Londres, ha estudiado la confianza en las vacunas en 67 países, con datos de 65810 voluntarios.
El sentimiento de confianza en las vacunas es general en todos los países estudiados, aunque hay mucha variabilidad en las respuestas a la encuesta de los autores. Es de destacar que la menor confianza se observa en Europa, con siete países europeos entre los diez que encabezan la lista de los que no se fían de las vacunas. En Francia, la desconfianza alcanza al 41% de los encuestados, seguida de Bosnia con el 36%. Los países con más confianza son Bangladesh, Ecuador e Irán y los más escépticos son Azerbaiyán, Rusia e Italia. La media de los 67 países es del 13% de falta de confianza en las vacunas. En España, el 28% no considera seguras las vacunas, y el 27% no cree que sean efectivas.
Los voluntarios con más confianza en las vacunas son los mayores de 65 años y los católicos. Y los que menos confianza tienen son de los países con más educación, mejor acceso a los servicios de salud y mayor estatus socioeconómico.
Todo este asunto de la falta de confianza, incluso del temor a las vacunas, comenzó en 1998 cuando Andrew Wakefield y su equipo, entonces en la Escuela de Medicina de Londres, publicaron un artículo que relacionaba la vacuna triple vírica, contra el sarampión, las paperas y la rubeola, con el autismo. Los resultados de este estudio provocaron miedo en los padres y un intenso debate público sobre la seguridad de la vacuna. Unos años, después, en 2010, se reunieron suficientes evidencias que demostraban que la publicación de Wakefield era un fraude e instituciones públicas y privadas la rechazaron. Incluso todos los firmantes del artículo original menos dos retiraron su apoyo al estudio. En 2017, Paul Offit, del Hospital Infantil de Philadelphia, escribe que el 85% de los padres de hijos autistas no creen que la vacuna sea la causa.
La revista The Lancet,que había publicado el artículo original de Wakefield en 1998, se retractó en 2017, y retiró el estudio de sus archivos. Y en 2011, la revista British Medical Journal publicó el relato de cómo se había gestado el fraude y el engaño de Wakefield.
Fue en 2014 cuando se publicó un meta análisis sobre lo conocido hasta esa fecha de la relación entre la vacuna triple vírica y el autismo, tal como Wakefield aseguraba en 1998. Fue el grupo de Luke Taylor, de la Universidad de Sydney, en Australia, quien revisó los trabajos publicados hasta abril de 2014. El total de la muestra son 1256407 niños y, además, se examinan otros cinco estudios con 9920 niños como control. Otra revisión, publicada en 2019, por el grupo de Anders Hviid, del Instituto Estatal del Suero de Copenhague, basada en el seguimiento de 657000 niños daneses, nacidos entre 1999 y 2010 y con un seguimiento hasta 2013, encuentra, también, que no hay relación entre la triple vacuna y el autismo.
Los resultados son claros: no hay relación entre la vacuna triple vírica y el autismo o con desórdenes que se asocian al autismo.
Andrew Wakefield perdió su licencia para ejercer la medicina. Pero el mito, en esos años, llegó a los medios y a las redes sociales y se extendió y, hoy en día, sigue vigente para muchas personas que siguen sin creer en las vacunas. En encuestas publicadas en Australia por el equipo de Stephan Lewandowsky, de la Universidad de Australia Occidental en Crawley, se encuentra que, en 2002, del 20% al 25% de la población cree en la relación entre la vacuna y el autismo, y del 39% al 53% considera que las evidencias a favor y en contra de esa relación están igualadas. Incluso un número relevante de profesionales sanitarios aceptan la relación.
Es interesante conocer las razones que llevan los antivacunas a seguir una conducta que el consenso científico afirma que puede ser peligrosa para la salud e, incluso, la vida de quien la sigue. El estudio de Beth Hoffman y su grupo, de la Universidad de Pittsburgh, utiliza datos que tienen un origen curioso, casi de serendipia. Este grupo de médicos publicó, en 2015, un video en Facebook recomendando el uso de la vacuna contra el virus del papiloma humano. En poco tiempo se convirtió en viral y recibió unas 10000 opiniones de 800 comentaristas de ocho países. La mayoría de los comentarios eran de contenido antivacunas, y los autores eligieron 197 comentaristas de los más activos.
El estudio de los textos permitió al grupo de Hoffman conocer las razones que apoyaban su ideología contra las vacunas. En primer lugar, está la desconfianza respecto a la comunidad científica. Después, aparecen los seguidores de terapias alternativas. En tercer lugar, los que aceptan las exageraciones del riesgo de las vacunas. Y, finalmente, están los conspiranoicos que acusan a gobiernos, instituciones y grandes empresas.
La persistencia de este mito ha llevado a Lewandowsky a investigar cómo se perpetúa. Se extiende por el entorno social, a veces sin ser nadie consciente de ello, ni de quien lo menciona ni quien lo acepta. Pero otras veces, muy a menudo, la difusión es a propósito. Son rumores que parten de obras de ficción, gobiernos, políticos, o de intereses creados. Internet es, en la actualidad, esencial para publicar, difundir y extender estas informaciones falsas y estos mitos. Si se pide en Google que busque “autismo vacuna relación” en inglés, las entradas son más de diez millones. Y, en un estudio publicado en 2018, el grupo liderado por David Bromatowski, de la Universidad George Washington de Washington DC, afirma que los contenidos antivacuna aparecen en gran cantidad en fabricantes de contenidos y trolls de Twitter difundidos desde Rusia.
El estudio de Carolina Moreno Castro, de la Universidad de Valencia, sobre las noticias publicadas en periódicos importantes, entre 2007 y 2013, sobre los beneficios y los riesgos de la vacuna contra el papiloma humano, aclara algunos comportamientos y, además, consiguen desconcertar al lector por las diferencias de orientación de los medios. Los siete diarios analizados son ABC, El Comercio, Las Provincias, Levante, La Nueva España, El País y El Mundo. Son 297 los textos localizados y analizados. Destacan los beneficios de la vacuna 149 artículos y previenen de los riesgos 127. Sin embargo, hay periódicos que publican más sobre riesgos: El Mundo, El País y Levante. Es el ABC el que más destaca los beneficios.
Estos periódicos, de gran tirada, influyen en la opinión pública y en la conducta de los ciudadanos respecto a esta vacuna. Aunque el número de noticias a favor y en contra sea parecido implica una cierta equidistancia, equivocada y poco científica, en la línea editorial de cada diario.
En la aceptación de la información falsa sobre las vacunas influye la ideología y las creencias previas e, incluso, la presentación de evidencias que demuestran la falsedad del mito lleva a algunas personas a reforzar sus creencias falsas. Son las famosas teorías conspiratorias de empresas farmacéuticas, gobiernos, sindicatos médicos, socialistas radicales y quien sabe que otro colectivo.
Es bueno, en el debate, presentar un relato alternativo y veraz; repetirlo cuantas veces sea necesario pero, siempre, con la precaución de no reforzar las falsedades y siempre basado en evidencias científicas; destacar la importancia básica que tienen los hechos; avisar y concretar qué informaciones falsas se van a tratar; utilizar pocos argumentos para rebatir la información falsa y recordar que, siempre, menos es más; ser crítico con las fuentes de informaciones falsas; reafirmar los datos verdaderos y relacionarlos con valores personales. No hay que olvidar el concepto de inmunidad colectiva que supone que no vacunarse pone en peligro la salud de las personas de la comunidad, y no solo de quien no se vacuna.
Referencias:
Broniatowski, D.A. et al. 2018. Weaponized health communication: Twitter bots and Russian trolls amplify the vaccine debate. American Journal of Public Health doi: 10.2105/AJPH.2018.304567
Deer, B. 2011. How the case against the MMR vaccine was fixed. British Medical Journal 342: 77-82.
EuroScientist. 2017. Vaccine successes. Facing diseases since the 18th century. 16 February.
Godlee, F. et al. 2011. Wakefield’s article linking MMR vaccine and autism was fraudulent. British Medical Journal 342: c7452.
Heap, M. 2019. Medicine on the fringe. Skeptical Intelligencer Spring: 4-5.
Hoffman, B.L. et al. 2019. It’s not all about autism: The emerging landscape of anti-vaccination sentiment on Facebook. Vaccine 37: 2216-2223.
Hviid, A. et al. 2019. Measles, mumps, rubella vaccination and autism. A nation wide cohorts study. Annals of Internal Medicine doi: 10.7326/M18-2101
Larson, H.J. et al. 2016. The state of vaccine confidence 2016: Global insights through a 67-country survey. EbioMedicine DOI: 10.1016/j.ebiom.2016.08.042
Lewandowsky, S. et al. 2012. Misinformation and its correction: Continued influence and successful debiasing. Psychological Science in the Public Interest 13: 106-131.
López Goñi, I. 2017. Dudas sobre las vacunas: problemas y soluciones. Cuaderno de Cultura Científica 12 junio.
Moreno Castro, C. 2015. La influencia de los medios de comunicación sobre el efecto Weber: correlación entre las noticias publicadas sobre la vacuna del VPH y las alertas registradas en farmacovigilancia. Panace@ 16: 195-205.
Offit, P. 2017. Las vacunas no causan autismo. Investigación y Ciencia enero: 40.
Taylor, L.E. et al. 2014. Vaccines are not associated with autism: An evidence-based meta-analysis of case control and cohort studies. Vaccine doi: 10.1016/j.vaccine.2014.04.085
Wakefield, A.J. et al. 1998. Ileal-lymphoid-nodular hyperplasia, non-specific colitis, and pervasive developmental disorder in children. Lancet 351: 637-641.
Wikipedia. 2017. Andrew Wakefield. 20 marzo.
Sobre el autor: Eduardo Angulo es doctor en biología, profesor de biología celular de la UPV/EHU retirado y divulgador científico. Ha publicado varios libros y es autor de La biología estupenda.
El artículo Desmitificando: Vacunas peligrosas se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Desmitificando: La vitamina C y el resfriado
- Desmitificando: Las rubias son “tontas”
- Dudas sobre las vacunas: problemas y soluciones
Un gen ahorrador
 Familia samoana residente en Australia. Foto: John Oxley Library, State Library of Queensland (Australia) / Wikimedia Commons.
Familia samoana residente en Australia. Foto: John Oxley Library, State Library of Queensland (Australia) / Wikimedia Commons.Sobre la obesidad actúan factores de naturaleza ambiental, pero también tiene una importante base genética. En las sociedades contemporáneas la actividad física ha disminuido con relación a la que se hacía en el pasado. Y a eso se añade la sobreabundancia de alimento fácil de digerir y absorber. Los mayores índices de sobrepeso y obesidad del mundo se dan en archipiélagos e islas del Pacífico, como Nauru o Kiribati (Micronesia), y Samoa, Tonga, Hawái o Tuvalu (Polinesia). Y lo llamativo de estos casos es que sus niveles de obesidad superan ampliamente los característicos de países con similar provisión de comida.
El sobrepeso se mide mediante el índice de masa corporal, que se calcula dividiendo el peso (en kg) entre el cuadrado de la altura (m). Si sobrepasa el valor de 25 indica sobrepeso, y si es mayor que 30, obesidad. En Samoa, uno de los archipiélagos citados, el valor medio de ese índice es 31’7, solo por debajo de los de la isla de Nauru (32’5) y el archipiélago de Tonga (31’9). A comienzos del siglo XXI, el 68% de los hombres y el 84% de las mujeres samoanas tenían sobrepeso; diez años después esos porcentajes habían subido al 80 y 91% respectivamente.
Hace cerca de seis décadas el genetista James Neel propuso que la diabetes tipo II podía ser una consecuencia negativa de la selección en la población de cierta variante genética, a la que él llamó “gen ahorrador”, que predispone a sus portadores a sufrir esa enfermedad. Más adelante, en la hipótesis se incluyó la obesidad como otra de sus consecuencias. La diabetes metabólica (tipo II) y la obesidad son rasgos que aparecen juntos a menudo, y lo que se proponía es que cierta variante genética podría haber sido beneficiosa en el pasado porque habría permitido sobrevivir con menos alimento, pero que en abundancia, lejos de ser beneficiosa, esa variante se convierte en un problema.
En un estudio reciente han encontrado que hay una fuerte asociación entre el índice de masa corporal y una mutación en el gen CREBRF, que es muy rara fuera de Samoa pero muy abundante en ese archipiélago. Aparte de esa relación, los investigadores hicieron experimentos con adipocitos (células que almacenan grasas de reserva) mediante las que observaron que la mutación en el gen CREBRF promueve un mayor almacenamiento de grasa y menor utilización de energía. Concluyeron, por tanto, que esa variante es, al menos en parte, responsable del sobrepeso de la gran mayoría de habitantes de Samoa. Por lo que la hipótesis “del gen ahorrador” se ha visto reforzada.
La mayoría de los genes que contribuyen a la obesidad lo hacen porque influyen en la regulación central (nerviosa y hormonal) del balance energético. El gen CREBRF, sin embargo, influye en el metabolismo celular. Y podría haber casos similares en otros grupos humanos.
Los samoanos, como otros polinesios, se han aventurado durante los últimos 3.000 años en grandes travesías oceánicas de duración y destino inciertos. Lo han podido hacer gracias al desarrollo del catamarán y a su gran pericia como navegantes. En esos viajes pasaron, con toda seguridad, hambre y frío. Solo quienes sobrevivían a esas duras condiciones han dejado descendencia. Y muchos de ellos sobrevivieron gracias a su metabolismo ahorrador. El pasado pasa ahora factura a los descendientes de aquellos navegantes en forma de obesidad generalizada, pues las condiciones a las que se ven expuestos los samoanos de hoy -alimento abundante y confort térmico- son diametralmente opuestas a las que tuvieron que superar sus ancestros. Un colofón nada épico a uno de los episodios más asombrosos de la odisea humana.
Fuente: Ryan L Minster et al (2016): A thrifty variant in CREBRF strongly influences body mass index in Samoans. Nature Genetics 48 (9): 1049-1054
Sobre el autor: Juan Ignacio Pérez (@Uhandrea) es catedrático de Fisiología y coordinador de la Cátedra de Cultura Científica de la UPV/EHU
El artículo Un gen ahorrador se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Andar puede salvarte la vida
- Obesidad y delgadez también se heredan
- #Naukas15 En el comer y en el rascar, ¿todo es empezar?
El color y sus orígenes

El color es algo que la mayoría damos por sentado, pero ¿qué es y cómo se origina? Si nadie las observa, ¿las cosas tienen color?
Para dar respuesta a estas cuestiones debemos acudir a diferentes ámbitos de la ciencia. Desde la cuántica a la neurociencia, pasando por la filosofía, se ha tratado de explicar uno de los fenómenos más fascinantes que tenemos delante de los ojos (¿o es detrás?). César Tomé López abordó esta cuestiones en la conferencia del ciclo Bidebarrieta Científica “El color y sus orígenes”, impartida el pasado 10 de abril en Biblioteca Bidebarrieta de Bilbao.
César Tomé López es el editor del Cuaderno de Cultura Científica y Mapping Ignorance, ambos medios de la Cátedra de Cultura Científica de la UPV/EHU. El divulgador, y químico industrial de formación, ha dedicado parte de su vida profesional a trabajar en distintas industrias relacionadas de una forma u otra con el uso técnico y comercial del color, desde fabricantes de pigmentos a empresas de alimentación. Además, Tomé López cuenta con un máster en Neurociencia y es el responsable de proyección internacional de Euskampus Fundazioa.
La charla se enmarca dentro del ciclo “Bidebarrieta Científica” una iniciativa que organizan todos los meses la Cátedra de Cultura Científica de la UPV/EHU y la Biblioteca Bidebarrieta para divulgar asuntos científicos de actualidad.
Edición realizada por César Tomé López
El artículo El color y sus orígenes se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Ciencia, arte y cultura callejera: física y música
- Los orígenes del arte
- Inmunoterapia contra el cáncer
Miles de nuevos cúmulos globulares en los últimos mil millones de años
 Imagen del telescopio espacial Hubble, en el que se ven los cúmulos globulares jóvenes en azul y los filamentos de gas frío en rojo en la galaxia NGC 1275 .
Imagen del telescopio espacial Hubble, en el que se ven los cúmulos globulares jóvenes en azul y los filamentos de gas frío en rojo en la galaxia NGC 1275 .Los cúmulos globulares pueden contener cientos de miles de estrellas, y hasta más de diez millones de ellas, que surgieron esencialmente al mismo tiempo. Se trata de los objetos visibles más ancestrales del universo. Los cúmulos globulares se aglutinan en densos volúmenes esféricos de diámetros cientos de veces más pequeños que el diámetro de nuestra galaxia. La Vía Láctea está rodeada de unos 150 cúmulos globulares, algunos de los cuales son visibles en la oscuridad de la noche; pero alrededor de las galaxias gigantes situadas en el centro de los cúmulos galácticos pueden encontrarse unos diez o veinte mil cúmulos globulares. Los cúmulos galácticos contienen cientos o miles de galaxias unidas por gravedad, e infundidas por gas caliente (más de diez veces más caliente que el que hay en el centro del Sol).
Se piensa que los cúmulos globulares se formaron poco después del nacimiento del universo, hace unos 13.800 millones de años, al mismo tiempo o puede que incluso antes que se formaran las primeras galaxias. Desde entonces se han mantenido inalterados en gran medida, aparte del envejecimiento de todas sus estrellas y de la progresiva muerte de la mayoría de las estrellas restantes.
Thomas Broadhurst, Ikerbasque Research Professor del Departamento de Física Teórica e Historia de la Ciencia de la UPV/EHU, ha explicado que “no se comprende muy bien por qué las galaxias más brillantes se forman en el centro de los cúmulos galácticos. Se cree que el hecho de que contengan miles de antiguos cúmulos globulares sea un punto a tener en cuenta”. Un estudio liderado por el Dr. Lim de la Universidad de Hong Kong y publicado en Nature Astronomy, en el que ha colaborado Broadhurst, ha encontrado respuestas inesperadas al origen de algunos cúmulos globulares situados alrededor de las galaxias gigantes en el centro de los cúmulos galácticos: “Hemos descubierto que miles de nuevos cúmulos globulares se han ido formando en los últimos mil millones de años a partir de un gas frío en la galaxia gigante situada en el centro del cúmulo galáctico Perseo”, explica el profesor Broadhurst.
Los cúmulos globulares más jóvenes están estrechamente asociados con —y en consecuencia están formados de— una compleja red de gas frío que se extiende hacia fuera de la galaxia gigante. Esta red de gas frío precipita del gas caliente que infunde todo el cúmulo galáctico Perseo; de hecho, el gas se concentra en el centro, permitiendo que se enfríe más rápidamente y eso da lugar a la creación de cúmulos globulares. Una vez formados, estos cúmulos globulares recién nacidos no se mantienen en la red de gas frío y llueven hacia el interior de la galaxia gigante, como gotas de lluvia que caen de las nubes. “Por lo tanto —explica Broadhurst—, cabe esperar que las galaxias centrales de estos cúmulos crecen en brillo a lo largo del tiempo cósmico, como consecuencia de la lluvia de cúmulos globulares que reciben del gas que les rodea”.
Referencia:
Jeremy Lim, Emily Wong, Youichi Ohyama, Tom Broadhurst & Elinor Medezinski (2019)Sustained formation of progenitor globular clusters in a giant elliptical galaxy Nature Astronomy doi: 10.1038/s41550-019-0909-6
Edición realizada por César Tomé López a partir de materiales suministrados por UPV/EHU Komunikazioa
El artículo Miles de nuevos cúmulos globulares en los últimos mil millones de años se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Los agujeros negros binarios en cúmulos globulares y Advanced-LIGO
- Constantes durante al menos 12 mil millones de años
- El análisis del supercúmulo «El Gordo» limita qué puede ser la materia oscura
Conversación fantástica con la de los cosméticos “sin tóxicos”

Nos citamos en una cafetería céntrica. Un roiboos con leche de soja, por favor. Dice leche. Para mí un café con leche, gracias.
—Me alegra que hayamos quedado.
—Hay muchas cosas que no estás contando bien, que no son como crees. Hay muchos intereses detrás. Así que quiero explicarte la verdad para que puedas hacer mejor divulgación.
—¿Cómo? ¿Me vas a explicar tú…? Sí, sí, claro, adelante, cuéntame LA VERDAD.
—Hay tropecientos ingredientes químicos permitidos en cosmética. De los cuales solo un porcentaje súper pequeño ha sido analizado. Súper pocos, eh. Y de esos, solo la mitad no son tóxicos. Pues con esos hacemos todos nuestros productos.
—Para, para. Esto no es así. Todos los ingredientes que se usan en cosmética están regulados. Hay una lista que figura en los anexos del reglamento donde especifican para qué sirven, en qué productos pueden estar, en qué cantidad… Y todo eso se sabe porque se han hecho ensayos toxicológicos para cada uno de ellos.
—¡Toxicológicos! Claro, porque son tóxicos. —Hace un gesto con la mano como diciendo ¿lo pillas?
—A ver. Un ensayo toxicológico se hace para identificar los peligros, cuantificar los riesgos y caracterizarlos. Se miden un montón de cosas. Mira. Primero, para identificar los peligros se hacen estudios in vivo e in vitro, se hacen ensayos clínicos, se mide la permeabilidad de la sustancia, la estabilidad… Después se cuantifican los riesgos por medio de tres variables, el SED (dosis de exposición sistémica), el NOAEL (los niveles sin efecto adverso observable) y el LOAEL (nivel mínimo de efecto tóxico observable). La relación entre el NOAEL y el SED nos da el MoS, que es el margen de seguridad. La concentración final calculada es la que se permite en cosmética. El riesgo es despreciable. Mira, te paso una infografía.
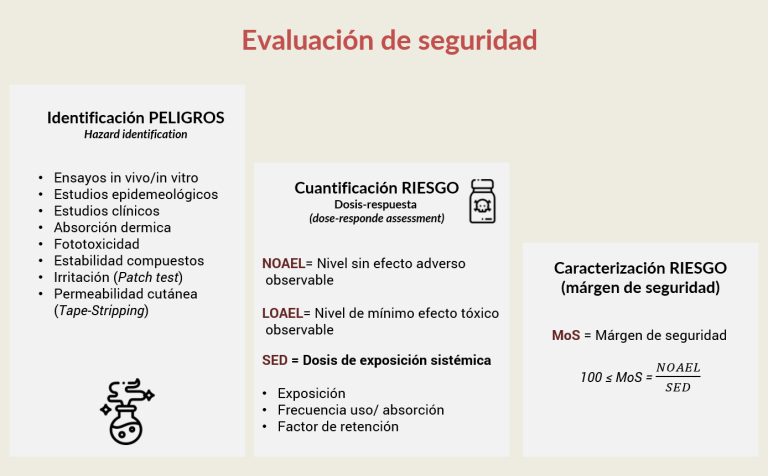 Fuente: Ciencia y Cosmética
Fuente: Ciencia y Cosmética—Sí, sí, lo que tú digas. Pero no se tiene en cuenta ni el efecto acumulativo ni el efecto cóctel.
—¡Claro que se tiene en cuenta! Es que es de cajón tenerlo en cuenta. A ver, que los que diseñan los ensayos toxicológicos lo habrán pensado, ¿no crees? Para la medida del NOAEL se realizan ensayos de evaluación por dosis repetidas a los 28 o 90 días e incluso años, dependiendo del tipo de cosmético, claro.
—Si todo fuese como tú dices, ¿por qué está permitido poner parabenos en los cosméticos? Es que clama al cielo. Que los parabenos son disruptores endocrinos y esto es muy tocho.
—Los parabenos no son disruptores endocrinos. Mira, te voy a pasar un enlace a un artículo de divulgación con todas las fuentes… ¿Sabes para qué sirven los parabenos?
—Y yo qué sé, chica. Están relacionados con el cáncer de mama porque son disruptores endocrinos. Y esto no lo digo yo, lo dice un señor que es médico. Publicó un libro y todo.
—Los parabenos son conservantes, se usan para preservar el producto de la degradación, que no se contamine y que sea seguro para nosotros. Si un cosmético no lleva parabenos como conservantes, llevará otros. Por seguridad. Los de tu marca “sin tóxicos” también llevan conservantes. De lo contrario no te permitirían comercializarlos.
—Mira, mira, espera—. Empieza a buscar en su móvil una imagen. —¡Mira esto!
—¿Qué quieres que vea ahí?
—Pues que estos son parabenos, ves, y esto otro es un estrógeno. Se parecen mogollón. Así que los parabenos son como estrógenos y eso es lo peor.
—Perdona que me ría, pero ¿en qué se parecen?
—Hexágonos, rayas… ¡Se parecen mazo, tía!
—Así es cómo se escriben las fórmulas químicas orgánicas, con rayas y hexágonos como tú dices. Pero es que una raya cambiada de sitio ya te da un compuesto totalmente diferente. Es que si tengo que explicarte esto, yo ya no sé… Mira por ejemplo el ibuprofeno, que ese seguro que lo conoces. El ibuprofeno es el ácido 2-(4-isobutilfenil)propiónico. Pues tiene dos formas, R y S. Una es como el reflejo en el espejo de la otra. Como nuestras manos. No se superponen. Pues esto ocurre con algunos compuestos. Se les llama enantiómeros. Pues resulta que el ibuprofeno tiene el enantiómero R y el S. Solo el S tiene actividad farmacológica. El otro no. —Busco en Google Imágenes “enantiómero ibuprofeno”—. Esta imagen me vale. Mira, estos sí que parecen iguales. ¿Ves alguna diferencia? Bueno, pues en nuestro cuerpo se comportan de forma totalmente diferente. Y ni siquiera tienen hexágonos ni rayas distintas.
—¿Y cómo me explicas que el médico este haya descubierto que los parabenos dan cáncer? Ahí te acabo de pillar, eh.
—Es que ese señor no ha descubierto nada. Si hubiese descubierto algo tendría que habérselo mandado a las autoridades sanitarias. Tanto la Agencia Española del Medicamento y del Producto Sanitario, que es quien regula los cosméticos, dice que son seguros en las dosis que se utilizan. Como el SCCS, que es el Comité Científico Europeo de Seguridad. O la mismísima Organización Mundial de la Salud. No ha descubierto nada.
—Esa es tu opinión.
—Es el consenso científico.
—¡Ja! Consenso dices. Eso está todo pagado por la industria, para que digan lo que ellos quieren.
—Si eliges creer en lo que dice un señor cualquiera, y ridiculizar a las autoridades sanitarias, a los científicos que trabajan en la industria cosmética… Yo ya no sé qué decirte. Es que crees que todo es una conspiración.
—No soy ninguna conspiranoica de esas, eh. Pero sé de buena tinta que hay cosas que se ocultan. Ese señor no es un señor cualquiera. Es médico. Y hay otra que también lo dice, que es médico también, creo.
—¿Para qué iba la industria a ocultar algo así? ¿Qué ganan?
—Poder seguir utilizando lo que les dé la gana, aunque sepan que da cáncer. Esto es así.
—¿Crees que quieren que todo el mundo enferme de cáncer? ¿En qué beneficia eso a la industria cosmética?
—A la cosmética a lo mejor no, pero a las farmacéuticas, que son todas una mafia, ya te digo que les viene genial tenernos a todos enfermos.
—Entonces sí que crees que hay una conspiración internacional de la industria farmacéutica. De todas las industrias farmacéuticas, que también han comprado al sector cosmético para enfermarnos a través del desodorante y del champú.
—Conspiración no sé, pero sí una mafia. ¡Solo quieren ganar dinero! Pasta, pasta—dice frotando los dedos.
—Creo que habría formas más efectivas de enfermar a un montón de gente sin tener que recurrir a poner tóxicos en los desodorantes.
—Bueno, yo te digo que no me fío. Y por eso mis productos no llevan esas sustancias químicas tóxicas. Ni parabenos, ni aluminio, ni sulfatos. Nada de químicos de esos.
—Llevan otras sustancias químicas que, a partir de cierta concentración también serían catalogadas como tóxicas. ¿Hacemos la prueba? Dime cualquier ingrediente al azar de uno de tus cosméticos “sin tóxicos” y busca en Google esa sustancia seguida de la palabra toxic. No se salvan ni la mitad. Afortunadamente la ciencia no funciona así. La evidencia científica no es el primer enlace que aparece en un buscador.
—Yo te digo lo que yo sé, que he investigado mazo estas cosas. Y doy charlas sobre esto y tengo mi marca que es súper guay porque es “sin tóxicos”.
—No es “sin tóxicos”. Es sin cultura, sin ética, sin ciencia. Y desgraciadamente las autoridades sanitarias están permitiendo que gente como tú haga ese tipo de publicidad. El Día Mundial Contra el Cáncer de Mama también aprovechaste para soltar que había sustancias en los cosméticos relacionadas con el cáncer de mama. Es indignante.
—¡Eh, eh, que puse una fuente de esas que tanto os molan a los de la ciencia! Lo dice el Cancer Research UK, eh, que eso es muy fuerte, tía.
—Ni siquiera te has leído tu propia fuente. El Cancer Research UK precisamente desmiente esos vínculos con el cáncer de mama. Ni los parabenos, ni el aluminio… Nada. Y eso ya es tan fácil como saber leer, chica.
—Lo vi en una infografía de Instagram. Mira que lo busco. Mira, mira.
—Una cuenta de Instagram de una ONG cualquiera, y además con solo 800 seguidores, no es una fuente fiable de información.
—Tú qué vas a decir, si a ti te paga la industria.
La invité al rooibos con bebida de soja y me marché.
*Nota de la autora:
Hace meses festejé que por fin se iba a acabar la cosmética “sin”. Había entrado en vigor un documento técnico que prohibiría este tipo de publicidad. Desgraciadamente se ha quedado en nada. No hay cambios. El Día Mundial Contra el Cáncer de Mama pudimos ver cómo de hecho esto va a peor. No quiero documentos técnicos como papel mojado. Quiero que se legisle de verdad. Que las malas prácticas publicitarias que atemorizan a los consumidores se persigan y se sancionen. Las autoridades sanitarias no pueden ser cómplices del engaño y la desinformación. Cuando uno cuenta con el respaldo de la información y del conocimiento, opinar es una forma de compromiso. Esta es mi opinión: hay que legislar.
Sobre la autora: Déborah García Bello es química y divulgadora científica
El artículo Conversación fantástica con la de los cosméticos “sin tóxicos” se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Adiós a las microesferas de plástico en los cosméticos
- Los cosméticos no se testan en animales
- Zientziateka: Blanca Mª Martínez García – La geología fantástica de Verne, Poe y H.P. Lovecraft
Si no me equivoco, 64=65
La paradoja de Curryi se produce al considerar el siguiente enunciado: «Si no me equivoco, B es verdad», es decir, «Si este enunciado es cierto, entonces B es verdad», dondeB puede ser cualquier declaración lógica, como ‘64=65’. Es decir, pensemos en la sentencia «Si no me equivoco, 64=65».
 Haskell Brooks Curry pensando en la paradoja que lleva su nombre. Composición realizada con la imagen del matemático obtenida de Wikimedia Commons.
Haskell Brooks Curry pensando en la paradoja que lleva su nombre. Composición realizada con la imagen del matemático obtenida de Wikimedia Commons.
Aunque 64 no sea igual a 65, el enunciado «Si no me equivoco, 64=65» es una sentencia en lenguaje natural, por lo que se puede analizar la verdad o falsedad de dicha oración. La paradoja se desprende precisamente de este análisis que consta de dos pasos:
-
se pueden usar técnicas de demostración en lenguaje natural comunes para demostrar que la sentencia «Si no me equivoco, 64=65» es verdadera;
-
la validez de «Si no me equivoco, 64=65» puede usarse para demostrar que 64=65. Pero, como 64 no es igual a 65, esto sugiere que ha habido un error en una de las pruebas.
La sentencia «Si no me equivoco, 64=65» podría ser reemplazada por cualquier otro enunciado, que también sería demostrable. Por lo tanto, cualquier sentencia parece ser demostrable. Como la prueba usa únicamente métodos de deducción aceptados y ninguno de estos métodos parece ser incorrecto, esta situación es paradójica.
Veamos una manera informal de probar la verdad de la sentencia «Si no me equivoco, 64=65». Se trata de un enunciado condicional, es decir, del tipo «Si A, entonces B», donde A de refiere al propio enunciado y B es ‘64=65′. El método usual para demostrar una proposición de este tipo («Si A, entonces B») es suponer la hipótesis cierta (A) y deducir la tesis (B). Supongamos por lo tanto que A es cierto. Pero A se refiere a la declaración completa –«no me equivoco», «este enunciado es cierto»–, es decir, si asumimos que A es cierto, también suponemos que se verifica «Si A, entonces B». De otro modo, si admitimos A, estamos aceptando al mismo tiempo «Si A, entonces B». Así, por modus ponendo ponens, B es verdad.
Así que el enunciado «Si no me equivoco, 64=65» ¡es cierto! Es decir, ¡64=65! ¿Qué no te lo crees? Compruébalo en riguroso directo:
Como has podido observar en el vídeo, la ‘supuesta’ demostración se inicia con un cuadrado de 8×8 unidades. Se trazan tres segmentos para dividirlo en dos triángulos rectángulos y dos trapecios rectángulos. Se recolocan estas cuatro piezas de manera conveniente y se obtiene un rectángulo de 13×5 unidades. Y se concluye, aparentemente, que 64=65.
Pero esto no es posible. ¿Cuál es el truco? Se han dibujado esos tres segmentos con un trazo suficientemente grueso para esconder lo que en realidad está pasando: se está ocultando un estrechísimo, casi imperceptible, trapezoide situado en la diagonal del rectángulo final, que tiene –como no podía ser de otra manera– área 1… ¡Las matemáticas no se equivocan!
Por cierto, la paradoja puede confirmarse usando diversas pruebas formales… y no parece tener una solución sencilla.
Referencias
-
Haskell Curry, Wikipedia (consultado el 26 de octubre de 2019)
-
Paradoja de Curry, Wikipedia (consultado el 26 de octubre de 2019)
iSe llama así por Haskell Brooks Curry (1900-1982), que fue un matemático y lógico estadounidense. Realizó su tesis doctoral –Grundlagen der kombinatorischen Logik, Fundamentos de la lógica combinatoria– en Gotinga bajo la supervisión de David Hilbert.
Su trabajo se centró fundamentalmente en lógica combinatoria, especialmente en la teoría de sistemas y procesos formales. Llevan su nombre los lenguajes de programación funcionales Haskell –debido a sus aportaciones al cálculo lambda–, Brook y Curry. En ciencias de la computación se denomina ‘currificación’ a una técnica para transformar funciones propuesta por los lógicos y matemáticos Gottlob Frege y Moses Schönfinkel y utilizada en programación funcional. Se llama correspondencia de Curry-Howard a la relación directa que guardan las demostraciones matemáticas y los programas informáticos –nombre que alude a Curry y William Alvin Howard–.
Sobre la autora: Marta Macho Stadler es profesora de Topología en el Departamento de Matemáticas de la UPV/EHU, y colaboradora asidua en ZTFNews, el blog de la Facultad de Ciencia y Tecnología de esta universidad.
El artículo Si no me equivoco, 64=65 se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:El modelo de Bohr explica la fórmula de Balmer
 Fuente: l’Observatoire de Paris
Fuente: l’Observatoire de ParisEl éxito más espectacular del modelo de Bohr fue que podía usarse para explicar todas las líneas de emisión (y absorción) en el espectro de hidrógeno; es decir, Bohr podía usar su modelo para derivar, y así explicar, la fórmula de Balmer para los espectros de hidrógeno.
Según el segundo postulado de Bohr, la radiación emitida o absorbida en una transición en un átomo debe tener una frecuencia determinada por hf = E1 – E2. Si nf es el número cuántico del estado final y ni es el número cuántico del estado inicial, entonces según el resultado para En: Ef = 1/nf2 · E1 y Ei = 1/ni2 · E1.
La frecuencia de la readiación emitida o absorbida cuando un átomo pasa del estado incial al final viene determinada por una relación muy simple que resulta de una manipulación muy sencilla de las igualdades anteriores:
hf = E1 · ( 1/ni2 – 1/nf2).
En la fórmula de Balmer aparecía la longitud de onda, no la frecuencia, por lo que usaremos la relación existente entre ambas variables. La frecuencia de una línea en el espectro es igual a la velocidad de la onda de luz dividida por su longitud de onda: f = c / λ. Sustituyendo f por c / λ en la última ecuación y luego dividiendo ambos lados por la constante hc (la constante de Planck multiplicada por la velocidad de la luz), obtenemos
1/λ = E1/ hc · ( 1/ni2 – 1/nf2).
Según el modelo de Bohr, entonces, esta ecuación proporciona la longitud de onda de la radiación emitida o absorbida cuando un átomo de hidrógeno cambia de un estado estacionario con número cuántico ni a otro con nf.
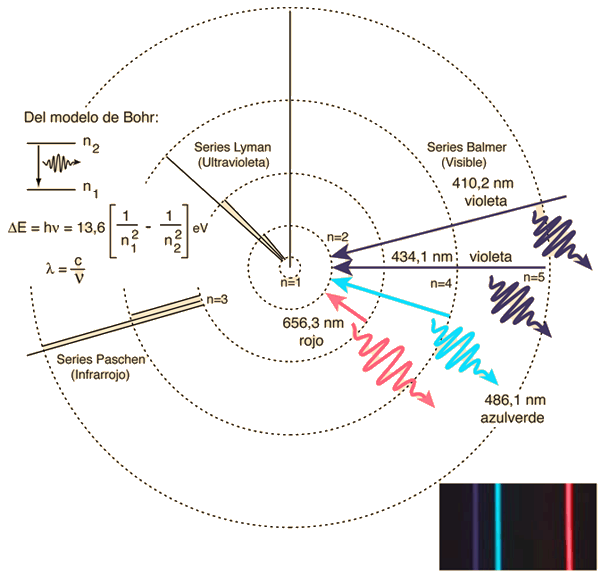 Fuente: Hyperphysics
Fuente: Hyperphysics¿Cómo se compara esta predicción del modelo de Bohr con la firmemente establecida fórmula empírica Balmer para la serie Balmer? Esta es, por supuesto, la pregunta crucial. La fórmula de Balmer, como ya vimos, en términos modernos es
1/λ = RH (1/22 – 1/n2)
Basta fijarse un poco para darnos cuentas de que la ecuación para la longitud de onda emitida (o absorbida) derivada del modelo de Bohr es exactamente la fórmula de Balmer siempre que nf = 2 y RH = – E1/ hc [1].
La constante de Rydberg RH se conocía desde hacía mucho tiempo por mediciones espectroscópicas que tenía un valor de 1,097 ·107 m-1. Ahora solo quedaba compararla con el valor que toma – E1/ hc [2]. La coincidencia era extremadamente buena. RH, hasta ese momento considerada como una constante determinada experimentalmente, ahora se demostraba que era un número que podía calcularse a partir de constantes fundamentales conocidas de la naturaleza: la masa y la carga del electrón, la constante de Planck y la velocidad de la luz.
Y lo que es más importante, ahora puedes ver el significado, en términos físicos, de la fórmula empírica para las líneas en la serie Balmer. Todas las líneas de la serie Balmer simplemente corresponden a transiciones de varios estados iniciales (varios valores de ni mayores que 2) al mismo estado final, para el que nf = 2. Por lo tanto, los fotones que tienen la frecuencia o la longitud de onda de la línea Hα se emiten cuando los electrones en un gas de átomos de hidrógeno «saltan» del estado n = 3 al estado n = 2; la línea Hβ corresponde a «saltos» de n = 4 a n = 2, y así sucesivamente.
Notas:
[1] Ojo al signo negativo.
[2] Recordemos que E1 tiene un valor negativo, por lo que – E1 es positivo.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
El artículo El modelo de Bohr explica la fórmula de Balmer se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:La CRISPR más precisa hasta la fecha convierte la tijera genética en una navaja suiza

Esta semana una nueva variante de la herramienta de edición genética CRISPR ha saltado a las primeras páginas de los periódicos, algo poco frecuente en noticias de ciencia. ¿Qué tiene de especial para haber despertado el interés de miles de investigadores?
Para responder a esta pregunta tengo que explicar un par de nociones básicas de genética molecular.
El ejemplo más acertado para ilustrar las capacidades de las herramientas CRISPR es una navaja suiza multiusos. Estas permiten desde pelar manzanas y atornillar hasta descorchar botellas.
En su versión más sencilla, una herramienta CRISPR está constituida por dos moléculas:
- Una proteína (Cas9), una nucleasa que corta el ADN en sus dos cadenas.
- Una pequeña molécula de ARN, el acido nucléico que actúa de intermediario entre el material genético que hay en el núcleo de la célula (ADN) y la producción de proteínas que ocurre fuera del núcleo, en el citoplasma de la célula.
Veamos qué hace cada componente.
El sentido de la vida
Lo normal es que la información genética progrese unidireccionalmente, desde el núcleo al citoplasma de la célula.
Una de las dos cadenas de ADN se copia en forma de ARN mediante un proceso que se llama transcripción. Este ARN sale al citoplasma y allí dirige la síntesis de una proteína determinada mediante un proceso que recibe el nombre de traducción.
Este flujo ADN -> ARN -> proteína es la base del funcionamiento de todas nuestras células.
Pero hace ya bastantes años se descubrió que existían unos virus, los retrovirus, que eran capaces de cambiar la dirección de ese flujo de información genética. Eran capaces de fabricar ADN a partir de ARN gracias a una nueva proteína que invertía el sentido de la ecuación. Dado que realizaba un proceso de transcripción al revés, se la bautizó como transcriptasa inversa.
 Proceso de transcripción y traducción.
Proceso de transcripción y traducción.Shutterstock/udaix
Cortar y pegar
En la versión más sencilla de CRISPR, la nucleasa Cas9 usa una pequeña molécula de ARN como guía para situarse en una posición concreta del genoma, sobre un gen determinado. Allí, tras realizar una última verificación, corta las dos cadenas de ADN.
Esto despierta los sistemas de reparación que se encargan de restaurar la continuidad del cromosoma. Por el camino obtenemos la edición o inactivación del gen deseado, según le aportemos o no un ADN molde que las proteínas reparadoras puedan usar para restaurar la secuencia.
Esto es la edición genética tradicional.
La tijera se convierte en lanzadera
¿Qué sucede si inhabilitamos la capacidad de corte de la Cas9 en una de las dos cadenas de ADN? Pues que solo cortará una de ellas. Esta Cas9 así modificada se llama nickasa y puede ser muy útil.
Si ahora inhabilitamos el corte de la otra cadena de ADN, la nickasa se convierte en una Cas9 muerta, incapaz de cortar el ADN. Pero seguirá localizándose en el lugar del genoma que la guía de ARN le indique: eso abre un mundo de oportunidades. Hemos convertido una tijera en una especie de lanzadera o módulo multiusos capaz de llevar la actividad que queramos a esa posición exacta del genoma. Bastará asociar esa nueva actividad a la nickasa o a la Cas9. El símil de la navaja multiusos cobra todo su esplendor.
El equipo de David Liu asoció, primero a una Cas9 inactiva y luego a una nickasa, una actividad denominada deaminasa, capaz de convertir una letra de la cadena de ADN en otra.
Con ello inventó en 2016 las variantes CRISPR llamadas “editores de bases”, capaces de cambiar determinadas bases del genoma de forma precisa. Con estos editores de bases se pensaba que podríamos tratar muchas enfermedades congénitas, al corregir las letras erróneas y substituirlas por las correctas, como si se tratara de un corrector molecular, como el famoso típex.
Sin embargo, su potencial quedó trastocado al descubrirse que se saltan el proceso de verificación de la secuencia sobre la cual se sitúan. Pueden ubicarse en muchos otros sitios del genoma, lo que produce numerosos cambios en genes que no deberíamos haber corregido y que darán resultados inesperados o no deseados.
Dos por el precio de uno
Esta semana Liu y sus colaboradores nos han vuelto a sorprender con su último trabajo publicado en la revista Nature. Esta vez han asociado una actividad transcriptasa reversa a una nickasa. En otras palabras, tenemos una proteína capaz de copiar ADN a partir de ARN en un sitio determinado del genoma.
¿Para qué podría servir? Pues para dirigir la copia de ADN que queremos producir según la información que contiene el ARN que actúa como molde.
¿Cómo hace para que el ARN actúe como molde? Muy sencillo. Se les ocurrió extender la pequeña molécula de ARN guía, que sirve para posicionar la nickasa en un sitio del genoma, y convertirla en una molécula bastante más larga. Ahora ese nuevo extremo puede usarse como molde para la otra cadena del ADN.
Eso es una propuesta muy inteligente que usa una misma molécula de ARN para dos cosas:
- Un extremo sirve para aparearse con una de las dos cadenas de ADN y así posicionar la Cas9 en el lugar deseado del genoma.
- El otro extremo sirve de molde para dirigir la síntesis de la otra cadena de ADN, la que hemos cortado. Podemos dirigir la síntesis a partir de la secuencia que le pongamos en ese nuevo extremo del ARN.
Así se pueden incorporar las letras correctas para corregir una mutación. O, al revés, generarla si se trata de saber qué pasa cuando ese gen está mutado.
Edición de calidad
A esta nueva capacidad de las herramientas CRISPR la han denominado “prime editing” (PE), que en inglés juega con el doble significado de “edición de calidad” y “guiada por un molde”.
Según sus autores, en teoría, se podrían corregir hasta un 89 % de los más de 75 000 errores genéticos que causan enfermedades en seres humanos. Estoy seguro de que ahora entienden mejor el grado de excitación que tenemos los investigadores con este nuevo “juguete”.
Lo que sabemos por ahora de las variantes PE es que funcionan en células humanas en cultivo, aunque no igual de bien con todos los tipos celulares. Se logran los cambios deseados con una buena eficiencia y, lo que es mejor, se reduce muchísimo la variabilidad de los resultados y la generación de mutaciones no deseadas en otras partes del genoma.
Pero todavía no sabemos si funcionará en animales y en personas. Tras la euforia inicial toca arremangarse. Muchos laboratorios de todo el mundo intentarán confirmar las buenas expectativas y con los nuevos experimentos iremos ampliando su potencial y descubriendo sus limitaciones.
Hay que celebrar esta nueva herramienta y felicitar a Liu y a sus colaboradores por su talento para combinar dos actividades (nickasa y transcriptasa inversa) que ni la evolución había asociado anteriormente. También ser prudentes: todavía no hemos curado ninguna enfermedad y puede que tardemos en hacerlo.![]()
Sobre el autor: Lluís Montoliu es investigador en Biología Molecular y Celular en el Centro Nacional de Biotecnología (CNB – CSIC)
Este artículo fue publicado originalmente en The Conversation. Artículo original.
El artículo La CRISPR más precisa hasta la fecha convierte la tijera genética en una navaja suiza se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Las herramientas de edición genética CRISPR y los ratones avatar
- La inminente revolución de la ingeniería genética basada en el sistema CRISPR/Cas
- Sobre la predisposición genética a padecer enfermedades (II)
La tabla periódica en el arte: Hierro
Se estima que el hierro supone el 95 % de la producción mundial de metales. No en vano lo necesitamos para realizar todo tipo de utensilios y construcciones. Pero este elemento no aparece en forma metálica en la corteza terrestre, sino formando diferentes de óxidos y sales. Tiene tal importancia que cuando aprendimos a extraerlo de la tierra se abrió una nueva era para la humanidad: la Edad del Hierro. Como no podría ser de otra forma, este elemento también ha tenido una gran trascendencia en la historia del arte. Pasen y vean.
Los pigmentos de la tierra
En algún momento remoto de nuestra prehistoria el ser humano tomó una piedra arcillosa para hacer uso de la primera pintura de color. Desde entonces la tierra nos ha regalado pigmentos que llamamos ocres y se han empleado en todos los rincones de nuestro planeta. El más conocido es el rojo y debe su color a la hematita, un óxido de hierro (Fe2O3). Este es probablemente el pigmento con la trayectoria de uso más longeva que existe. Desde el primitivo arte rupestre a los movimientos vanguardistas ha sido empleado sin interrupción. Pero los ocres van mucho más allá del rojo y ofrecen una gama de colores amarillos, pardos, negruzcos e, incluso, morados. Usamos el término ocre para referirnos a pigmentos que contienen óxidos e hidróxidos de hierro y suelen estar mezclados con arcilla y otros minerales. Estos compuestos proceden de rocas ricas en hierro, por lo que son muy abundantes en la naturaleza y dan lugar a paisajes extraordinarios como los de Rousillon (Francia) o la montaña de los siete colores (Perú).
 Imagen 1. Algunos de los colores de la montaña Winikunka provienen de compuestos con hierro. Fuente: Oskar González
Imagen 1. Algunos de los colores de la montaña Winikunka provienen de compuestos con hierro. Fuente: Oskar González
La transcendencia de estos compuestos a lo largo de toda la historia del arte viene, en gran medida, propiciada por la facilidad con la que se pueden obtener. De hecho, por su origen, también se les llama “tierras”. Entre estas tierras destacan, además del rojo, el ocre amarillo y el ocre marrón, cuyos colores se deben a un oxihidroxido de hierro (FeO(OH)) que forma minerales como la goethita y la limonita. Si abrimos el espectro, encontraremos pigmentos como la siena o la sombra, de tonos más marrones por la presencia de manganeso. Este elemento también podría explicar por qué en ciertas cuevas existen pinturas rupestres de color morado, como el llamativo caballo violeta de Tito Bustillo (Asturias).
Vemos, por tanto, que esta familia de pigmentos ofrece un arcoíris de colores que el ser humano ha empleado antes incluso de que existiese el arte. Por hacer un fugaz recorrido por obras emblemáticas que contienen estos pigmentos ricos en hierro diremos que decoraban los techos de la cueva de Altamira y los frescos del palacio de Cnosos, que tiñen el manto del San Sixto de Rafael y el cabello de las mujeres de Modigliani, que enrojecen los cuadros de Degas y que todavía llenan de color el arte de los artistas aborígenes contemporáneos.
 Imagen 2. Algunas de las grandes obras de arte que incluyen ocres. Fuente: Imágenes obtenidas de Wikimedia Commons y National Gallery of Victoria.
Imagen 2. Algunas de las grandes obras de arte que incluyen ocres. Fuente: Imágenes obtenidas de Wikimedia Commons y National Gallery of Victoria.
Un nuevo azul
El azul es un color esquivo. Escasea en la naturaleza y los pigmentos de uso histórico que se obtenían de minerales o plantas como el índigo eran caros o inestables. Por fortuna, a principios del s. XVIII apareció el que muchos consideran el primer pigmento moderno: el azul de Prusia. Un azul que era más intenso y menos fugaz que sus predecesores naturales. Tuvo tal éxito que llegó incluso al país del sol naciente de la mano de los comerciantes holandeses. Allí, el gran Hokusai lo empleó para elaborar la más famosa pieza de ukiyo-e (estampas realizadas con grabados en madera): La gran ola de Kanagawa. Una metáfora excelente de cómo el nuevo producto se extendía por el mundo. Más allá de su importancia artística, el azul de Prusia fue el protagonista de uno de los casos de serendipia más hermosos de la historia del arte y la ciencia, ya que fue descubierto por Johann Jacob Diesbach cuando realmente quería lograr una laca roja.
 Imagen 3. La gran ola de Kanagawa (26×38 cm), de Hokusai (1829-33).
Imagen 3. La gran ola de Kanagawa (26×38 cm), de Hokusai (1829-33).
Además de su uso como pigmento artístico, el azul de Prusia propició la aparición de un procedimiento fotográfico de gran transcendencia para el mundo científico: la cianotipia, del griego kyáneos (azul marino). Esta técnica fue inventada por John Herschel (hijo del astrónomo William Herschel y sobrino de la también astrónoma Caroline Herschel) a mediados del s. XIX, aunque fue su amiga Anna Atkins quien supo sacarle partido realizando impresiones de algas y publicando el que se considera el primer libro ilustrado con fotografías: Photographs of British Algae. Atknis enseguida comprendió el valor de la invención de Herschel, que supuso un antes y un después en la documentación botánica.
 Imagen 4. Furcellaria fastigiata en Fotografías de algas británicas de Anna Atkins (1844). Fuente: The New York Public Library
Imagen 4. Furcellaria fastigiata en Fotografías de algas británicas de Anna Atkins (1844). Fuente: The New York Public LibraryPor último, tranquilizaremos a quien tras leer sobre el uso de ferrocianuros piense que el azul de Prusia es un poderoso veneno diciendo que, al encontrarse el cianuro fuertemente unido al hierro, no resulta tóxico. Al contrario, este compuesto es un antídoto contra el envenenamiento por talio o cesio radioactivo.
Tintas ricas en taninos
Algunos dibujos de Rembrandt, los primeros bocetos de la constitución de Estados Unidos, las partituras de Bach o los cuadernos de Leonardo da Vinci tienen algo en común: la tinta ferrogálica. La que posiblemente sea la tinta más importante de la historia de Occidente se usó desde la época del Imperio Romano hasta el s. XX, cuando las tintas sintéticas la fueron desplazando. Su carácter indeleble la hizo especialmente útil para escribir documentos, no en vano en Alemania fue empleada de forma oficial por el gobierno hasta los años 70. Pero, ¿qué es la tinta ferrogálica? ¿De dónde se obtiene?
La receta de las tintas ferrogálicas consiste en mezclar cuatro ingredientes: sulfato de hierro (FeSO4), taninos, goma arábiga y agua. El ingrediente más peculiar son los taninos, que se lograban principalmente de las protuberancias que surgen en algunos árboles como respuesta al ataque de insectos. Esa especie de bolas se conocen como agallas, palabra que proviene del latín galla y explica parte de la etimología de la tinta. Las agallas son una fuente excelente de ácido tánico, substancia que se extrae tras un proceso de fermentación o empleando ácidos para que el proceso sea más eficiente. De la hidrólisis de este ácido se obtiene ácido gálico, compuesto que tras reaccionar con el hierro da lugar a la tinta ferrogálica.
 Imagen 5. La agalla de un árbol, fuente tradicional de taninos. Fuente: Wikimedia Commons.
Imagen 5. La agalla de un árbol, fuente tradicional de taninos. Fuente: Wikimedia Commons.
La fuente de hierro era el sulfato de hierro (II), conocido como vitriolo, una sal que se obtenía de la minería y era de gran importancia por ser la materia prima necesaria para lograr ácido sulfúrico. Por último, la goma arábiga es un producto obtenido de las resinas de ciertas acacias que juega un papel vital en el mundo del arte, por ejemplo como aglutinante en acuarelas. Esta goma rica en polisacáridos es soluble en agua (el cuarto ingrediente) y permite mantener en suspensión el pigmento, además de otorgar al líquido la viscosidad necesaria. Una vez realizada la mezcla, ésta se deposita sobre el papel, de modo que, gracias a su solubilidad en agua, el complejo formado por los taninos y el hierro (II) penetra en el soporte. El color de la tinta en ese momento es muy tenue, pero con la exposición al aire el hierro (II) se oxidará a hierro (III) y, poco a poco, se formará un compuesto insoluble de color oscuro.
Le rouge et le noir
El óxido de hierro presente en la tierra no sólo ofrece pigmentos, sino que posibilita una de las manifestaciones artística más interesantes desde el punto de vista químico: la cerámica griega. Esa cerámica en la que se combinan rojo y negro y que en tantos museos habréis podido contemplar, ya que los intrépidos griegos dejaron vestigios por todo el Mediterráneo. Podríamos pensar que los dibujos se realizan pintando sobre la arcilla cocida, pero lo cierto es que el proceso es mucho más complejo. Por una parte, los griegos empleaban arcilla ática, rica en óxidos de hierro y, por otra parte, un engobe fundente: una pasta de arcilla que a la postre daría el color negro vidrioso. Así, el artista aplicaba este engobe sobre las partes que debían de quedar de color oscuro, mientras que las partes rojas se lograrían dejando la cerámica al descubierto. Una vez realizado el dibujo, la pieza se introducía en el horno. En un proceso de tres etapas (oxidación-reducción-oxidación) se jugaba con el estado de oxidación de la arcilla y el engobe para lograr la combinación cromática deseada. Este fue el fundamento de la cerámica griega en la que destacan dos técnicas diferentes: la cerámica de figuras negras y la de figuras rojas.
 Imagen 6. Cerámica de figuras rojas conocida como La Piedad de Memnon (Ø 27 cm) (ca. 490 a.e.c.). Fuente: Wikimedia Commons.
Imagen 6. Cerámica de figuras rojas conocida como La Piedad de Memnon (Ø 27 cm) (ca. 490 a.e.c.). Fuente: Wikimedia Commons.
Cuando el hierro se convierte en arte
El hierro es el metal más abundante del universo y del núcleo de nuestro planeta. Esto es debido a que es el último producto que pueden formar las estrellas mediante fusión nuclear con un rendimiento positivo (los elementos más pesados sólo se generan si se forman supernovas). De hecho, podemos decir que los primeros objetos que el ser humano pudo elaborar con hierro metálico son regalos de las estrellas en forma de meteorito. Uno de los más célebres es la daga encontrada en la tumba de Tutankamón que data del s. XIV a.e.c., un par de siglos antes de que el ser humano dominase la fundición del hierro. Esta daga ha dado mucho que hablar, pero los últimos estudios realizados con fluorescencia de rayos X parecen confirmar su origen extraterrestre basándose en la cantidad de níquel y la proporción de níquel/cobalto.
Pese a su abundancia en la corteza terrestre, el hierro no aparece en forma metálica, sino formando compuestos con otros elementos (como los ocres que acabamos de ver). Si a eso le sumamos su alto punto de fusión (1538 ⁰C) y la mayor facilidad para usar el bronce, comprenderemos por qué el ser humano no aprendió a manipular este metal hasta el 1200 a.e.c.. Desde entonces, bien sea como hierro forjado o como acero (la aleación que forma con el carbono), es el metal por excelencia para la manufactura de todo tipo de objetos. Así, el hierro se ha empleado para elaborar tanto monumentales piezas de rejería como esculturas, siendo algunas de las más conocidas las de Chillida, Oteiza o, más recientemente, Jaume Plensa.
 Imagen 7. Construcción con tres cuboides vacíos (48x52x77 cm), de Oteiza (1958) Fuente: Artium.
Imagen 7. Construcción con tres cuboides vacíos (48x52x77 cm), de Oteiza (1958) Fuente: Artium.
Arquitectura en hierro
Pese a la gran abundancia de minerales con hierro, este metal no se pudo usar para la realización de grandes obras hasta la Revolución Industrial, momento en el que se desarrollaron procesos para lograr hierro fundido en grandes cantidades. El s. XIX es el de la consolidación de la arquitectura en hierro, un periodo en el que se abre la posibilidad de emplear este material resistente al fuego como alternativa a la piedra y la madera. Al principio se usó exclusivamente en arquitectura industrial, pero pronto se fue expandiendo su uso en todo tipo de edificios gracias a su relativo bajo coste, su mencionada resistencia y la posibilidad de construir rápidamente. El hierro permitió nuevas tipologías constructivas de gran tamaño y fue usado para realizar puentes y estructuras de edificios como mercados o estaciones de tren.
La forma más importante para lograr grandes volúmenes de hierro con las propiedades mecánicas requeridas era el pudelado, un proceso en el que el metal fundido se bate dentro de un horno para que el carbono y el azufre entren en contacto con el aire y puedan arder. Sin lugar a dudas, la obra de ingeniería más conocida realizada con este material es la torre Eiffel, construida para la Exposición Universal de 1889. Pese a que han pasado más de 130 años desde entonces hay datos que siguen siendo sorprendentes: se emplearon 7 341 toneladas de hierro para realizar 18 038 piezas metálicas y 2 500 000 remaches, se construyó en poco menos de dos años y la cúspide no oscila más de siete centímetros. Con razón dijo monsieur Eiffel que la bandera francesa era la única que poseía un mástil de 300 metros.
Como decíamos, el hierro también se ha empleado en la construcción de puentes, entre los que podemos destacar el Puente Colgante de Portugalete. Esta es la construcción de hierro más emblemática del País Vasco y la única declarada patrimonio de la humanidad por la UNESCO. La obra fue inaugurada en 1893 (sólo cuatro años después que la archiconocida torre) y es, hoy en día, el puente transbordador más antiguo que existe. Esta construcción única salva la ría del Nervión con sus 160 metros de longitud y sus 61 metros de altura.
 Imagen 8. El Puente Colgante de Portugalete (o Puente Bizkaia). Fuente: Wikimedia Commons.
Imagen 8. El Puente Colgante de Portugalete (o Puente Bizkaia). Fuente: Wikimedia Commons.
Para saber más:
P.A. Saura. El Amanecer del Arte. Universidad Complutense de Madrid (2017).
E. Alegre Carvajal et al. Técnicas y Medios artísticos. Editorial Universitaria Ramón Areces (2011).
Sobre el autor: Oskar González es profesor en la facultad de Ciencia y Tecnología y en la facultad de Bellas Artes de la UPV/EHU.
El artículo La tabla periódica en el arte: Hierro se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- La tabla periódica en el arte: Cobre
- La tabla periódica en el arte: Titanio
- La tabla periódica en el arte: Arsénico
Ageing-On: Promoviendo un envejecimiento saludable y estimulante para todas las personas

Actualmente, las personas mayores constituyen la población de más rápido crecimiento a nivel mundial. Según datos del informe “Perspectivas de la Población Mundial” de las Naciones Unidas, se espera que el número de personas de 60 años o más se duplique para 2050 y triplique para el año 2100: de 962 millones en 2017 a 2100 millones en 2050 y 3100 millones en 2100.
En Euskadi, la población mayor de 65 años ya representa el 22% total de la población. En este contexto, cada vez son más las políticas y acciones concretas que se ponen en marcha con el objetivo de promover un envejecimiento activo y conseguir en la vejez la mayor calidad de vida posible.
Este es precisamente uno de los cometidos del grupo de investigación Ageing-On de la Universidad del País Vasco (UPV/EHU), dirigido por el doctor Jon Irazusta y compuesto por especialistas con formación multidisciplinar. En concreto, el principal objetivo del equipo es mejorar la calidad de vida de las personas mayores mediante su participación en programas de ejercicio físico y cognitivo adaptados a las necesidades de cada persona.
La doctora en Bioquímica y Biología Molecular por la UPV/EHU e investigadora de Ageing-On Begoña Sanz se encargó de presentar el trabajo de este grupo y las ventajas de este tipo de programas en la conferencia titulada “Ageing On: Promoviendo un envejecimiento saludable y estimulante para todas las personas”, que se celebró el pasado 30 de enero en la Biblioteca Bidebarrieta de Bilbao.
La investigadora explica cómo esta tipología de programas de ejercicio influyen en la mejora física, cognitiva y psicológica de los participantes y analiza el papel fundamental que juegan estos entrenamientos en el envejecimiento saludable.
Begoña Sanz, que actualmente es profesora agregada del Departamento de Fisiología de la UPV/EHU, desarrolla su labor docente en el Grado de Medicina, en el Máster de Investigación Biomédica y en el Máster de Envejecimiento Saludable y Calidad de Vida de la UPV/EHU. Su trayectoria investigadora está ligada al estudio de biomarcadores moleculares, uno de los parámetros que se investiga en el grupo de investigación Ageing-On.
La charla se enmarca dentro del ciclo “Bidebarrieta Científica” una iniciativa que organiza todos los meses la Cátedra de Cultura Científica de la UPV/EHU y la Biblioteca Bidebarrieta para divulgar asuntos científicos de actualidad.
Edición realizada por César Tomé López
El artículo Ageing-On: Promoviendo un envejecimiento saludable y estimulante para todas las personas se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- El método Feldenkreis y las personas con discapacidad intelectual
- Vida saludable contra la diabetes
- #Naukas14 Espadas romanas para detectar materia oscura
El oso de las cavernas
Asier Gómez & Mónica Villalba
El oso de las cavernas (Ursus spelaeus s.l.) es una de las especies paradigmáticas de la megafauna cuaternaria (Figura 1). Existió desde el final del Pleistoceno Medio y durante el Pleistoceno tardío hasta que desapareció hace entre 24 y 26 mil años, en mitad de un estadial frío. La causa de su extinción es aún objeto de debate, pero las hipótesis más aceptadas proponen, por un lado, un descenso de la productividad de la vegetación a causa del enfriamiento del clima, y por otro, la caza por parte del ser humano. Algunos autores plantean la pervivencia de esta especie en refugios climáticos en el sur y en el este de Europa durante algunos miles de años más, pero hacen falta nuevas dataciones de carbono 14 para poder corroborarlo. Los estudios paleogenéticos indican que coexistieron, al menos, cuatro linajes genéticos dentro de los osos de las cavernas del Pleistoceno tardío. De hecho, algunos científicos llegan a nombrarlos como especies distintas: Ursus ingressus del centro y este de Europa, Ursus kudarensis del Caúcaso, Ursus rossicus del sur de Siberia) (Figura 2).
 Figura 1. Reconstrucción de un oso de las cavernas. Dibujo realizado por Amaia Torres Piñeiro.
Figura 1. Reconstrucción de un oso de las cavernas. Dibujo realizado por Amaia Torres Piñeiro.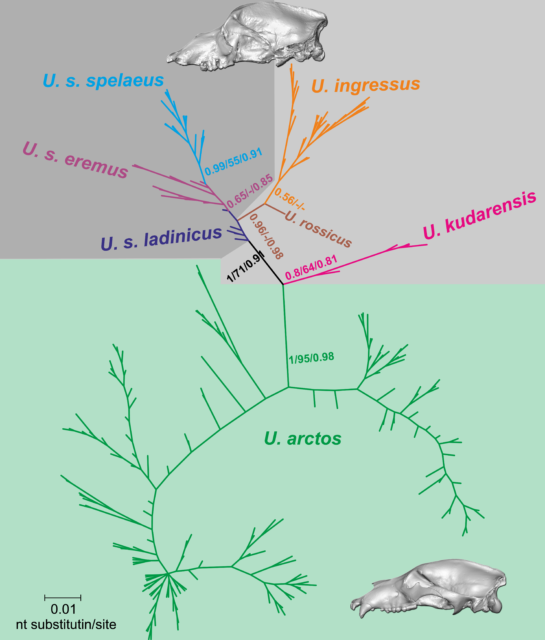 Figura 2. Mapa filogenético del grupo de los osos de las cavernas (arriba; cuatro especies, una de ellas con dos subespecies) en relación con el oso pardo (abajo). Modificado de Baca et al. (2016).
Figura 2. Mapa filogenético del grupo de los osos de las cavernas (arriba; cuatro especies, una de ellas con dos subespecies) en relación con el oso pardo (abajo). Modificado de Baca et al. (2016).
Su descripción como nueva especie fue realizada por Johann Christian Rosenmüller en 1794. Su nombre deriva de que los primeros fósiles de osos de las cavernas fueron encontrados en cuevas. En algunas cavidades de Europa se han descubierto acumulaciones de miles de huesos debido a que esta especie usaba las cuevas como lugar de hibernación, y a veces morían de inanición en ellas.
Existen diferencias notables cuando se compara el oso de las cavernas a su pariente vivo actual más cercano: el oso pardo. Estas diferencias se pueden encontrar en todas las regiones esqueléticas pero son notables en el cráneo, mandíbula (Figura 3) y en las manos y pies. En estas últimas regiones, el dedo I (el pulgar) es más corto en los osos de las cavernas. Además, tanto sus metápodos como sus falanges son más robustas, es decir más anchas en comparación con su longitud.
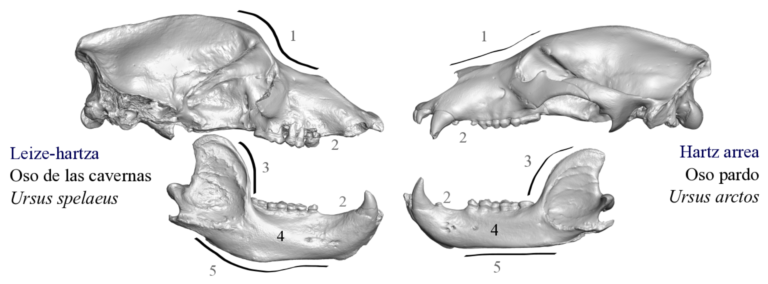 Figura 3. Existen numerosas diferencias entre los osos de las cavernas y los osos pardos (que presentan un patrón morfológico más primitivo). Los osos de las cavernas muestran un marcado escalón en la frente (1), han perdido los premolares más pequeños en el maxilar y en la mandíbula (2), presentan una rama mandibular adelantada (3), con un cuerpo mandibular más alto (4) y con un perfil más curvo (5). La mayor parte de estas diferencias, junto con la presencia de dientes más grandes, están relacionadas con la dieta más vegetariana de los osos de las cavernas. Figura: Asier Gómez/Mónica Villalba. Licencia Creative Commons 4.0.
Figura 3. Existen numerosas diferencias entre los osos de las cavernas y los osos pardos (que presentan un patrón morfológico más primitivo). Los osos de las cavernas muestran un marcado escalón en la frente (1), han perdido los premolares más pequeños en el maxilar y en la mandíbula (2), presentan una rama mandibular adelantada (3), con un cuerpo mandibular más alto (4) y con un perfil más curvo (5). La mayor parte de estas diferencias, junto con la presencia de dientes más grandes, están relacionadas con la dieta más vegetariana de los osos de las cavernas. Figura: Asier Gómez/Mónica Villalba. Licencia Creative Commons 4.0.
El tamaño de los osos de las cavernas sería similar al de los osos de mayor tamaño actuales (oso Kodiak y oso polar) con medias rondando los 400-500 kg para los machos y 225-250 kg para las hembras. Esta diferencia de tamaño entre ambos sexos se denomina dimorfismo sexual. Este dimorfismo es también observable en el tamaño de los huesos individuales, que también pueden presentar diferencias notables. Habitualmente, debido a que la dentición se preserva mejor en el registro fósil, se suelen usar las dimensiones transversales del canino para distinguir entre machos y hembras. En esqueletos completos, también sería posible distinguir los osos machos por la presencia del báculo (o hueso peneano), hueso presente en los machos de muchos grupos de mamíferos, en contraposición del baubellum (o hueso clitoriano) presente en las hembras. Las diferencias de tamaño también se dieron entre diversas poblaciones de osos de las cavernas. Por ejemplo, algunos restos hallados en los Alpes orientales (Ursus spelaeus lanidicus y Ursus spelaeus eremus) muestran notables diferencias con el resto de poblaciones por su menor tamaño. Por otro lado, uno de los linajes de oso de las cavernas, Ursus ingressus, que habitó el centro y el este de Europa presenta un mayor tamaño y robustez que los osos de las cavernas occidentales (Ursus spelaeus s.s.).
Su distribución fue muy extensa y comprendía toda Europa y parte de Asia (el Caúcaso y Siberia) (Figura 4). En la península ibérica sólo se ha documentado en la mitad norte, siendo especialmente abundantes los yacimientos y número de restos en la cornisa cantábrica y noreste de Cataluña (Figura 5).
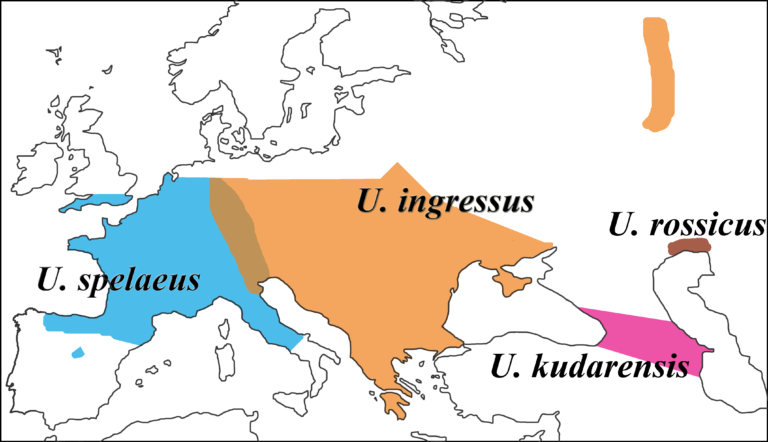 Figura 4. Mapa de Europa donde se muestran las distintas especies de osos de las cavernas propuestas y su distribución geográfica. Figura: Mónica Villalba/Asier Gómez. Licencia Creative Commons 4.0.
Figura 4. Mapa de Europa donde se muestran las distintas especies de osos de las cavernas propuestas y su distribución geográfica. Figura: Mónica Villalba/Asier Gómez. Licencia Creative Commons 4.0.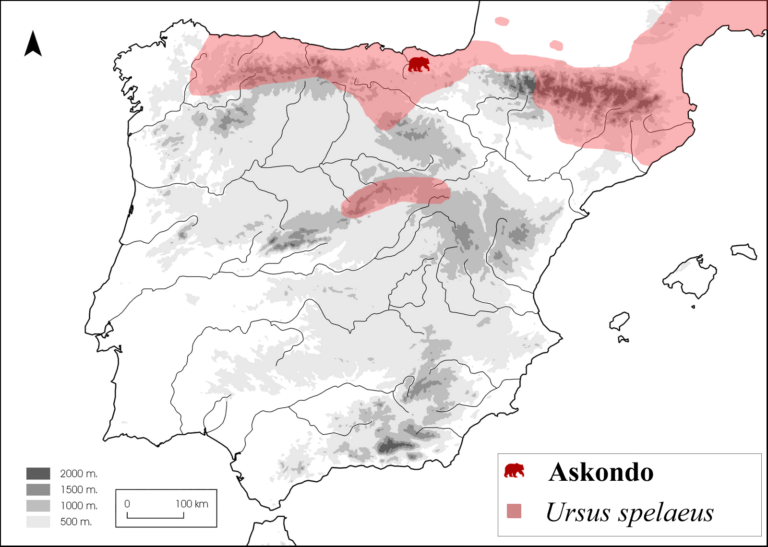 Figura 5. Localización de Askondo y área de distribución de osos de las cavernas en la península ibérica. Figura: Mónica Villalba/Asier Gómez.
Figura 5. Localización de Askondo y área de distribución de osos de las cavernas en la península ibérica. Figura: Mónica Villalba/Asier Gómez.
En el País Vasco se han encontrado grandes acumulaciones de esta especie en Muniziaga (Galdames), Askondo (Mañaria), Astigarragako kobea y Ekain (Deba), Lezetxiki (Arrasate), Troskaeta (Ataun), Arrikrutz (Oñati), Amutxate (Aralar), e Isturitz (Izturitze), entre otros.
El linaje de los osos de las cavernas y de los osos pardos tienen un origen común hace más de 1,2 millones de años, de acuerdo con estudios moleculares. Su ancestro más inmediato sería el oso de Deninger (Ursus deningeri), que presenta una morfología similar, pero de menor tamaño y robustez que sus descendientes (Figura 6). La división entre ambas especies es artificial ya que presentan muchas formas intermedias y, por ello, muchos autores los engloban dentro del grupo de los osos de las cavernas. En Bizkaia se han recuperado restos muy completos de U. deningeri en la cueva de Santa Isabel de Ranero (Karrantza) con una antigüedad de unos 300 mil años (Figura 7).
Durante el Pleistoceno Medio y tardío en Europa, los osos de las cavernas convivieron con otras especies de oso, como por ejemplo el oso pardo (Ursus arctos) y puntualmente con el oso negro tibetano (Ursus thibetanus). A pesar de ser linajes distintos, los estudios genéticos han demostrado que los osos de las cavernas y los osos pardos hibridaron ya que el oso pardo actual preserva entre un 0,9 y un 2,4% de su genoma proveniente de la especie extinta.
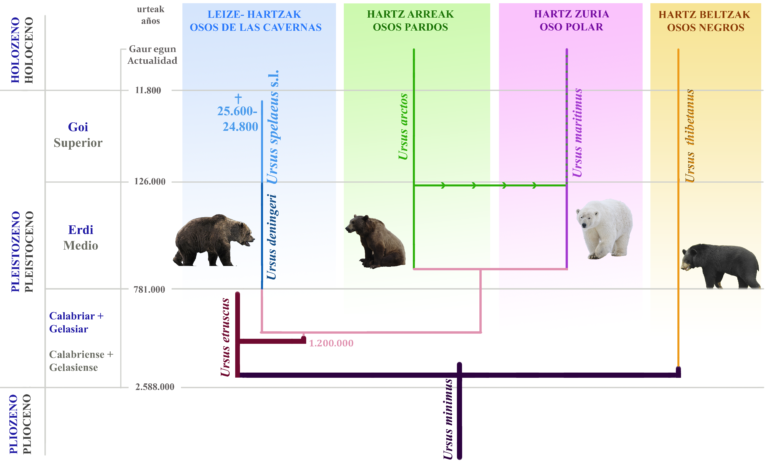 Figura 6. Esquema evolutivo simplificado en el que se muestra la relación del oso de las cavernas con algunos de los osos actuales. Figura: Mónica Villalba/Asier Gómez.
Figura 6. Esquema evolutivo simplificado en el que se muestra la relación del oso de las cavernas con algunos de los osos actuales. Figura: Mónica Villalba/Asier Gómez. Figura 7. Dibujo del cráneo de Ursus deningeri de Santa Isabel de Ranero (Karrantza). Dibujo por Paula Martin Rodríguez.
Figura 7. Dibujo del cráneo de Ursus deningeri de Santa Isabel de Ranero (Karrantza). Dibujo por Paula Martin Rodríguez.
Estudios recientes describen que su dieta era principalmente herbívora (frutos, hierbas, raíces, bayas, etc) en base a estudios isotópicos, y de la morfología del cráneo, la mandíbula y la dentición. Los osos de las cavernas pierden los premolares anteriores, de menor tamaño, y desarrollan dientes más grandes y multicuspidados que resultaron en una mayor superficie total de trituración adaptada a la ingesta de alimentos abrasivos. Además, la mandíbula es más robusta que en otras especies de oso y presenta profundas superficies de inserción muscular para unos desarrollados músculos de la masticación. Por otro lado, algunos restos fósiles muestran marcas de dientes que indican que fueron carroñeados por otros osos de las cavernas, y estudios sobre el microdesgate de los osos indican que su dieta podría ser más amplia y llegar a consumir carne. Por tanto, estos osos, sin llegar a ser tan omnívoros como los osos pardos, tampoco serían herbívoros estrictos. Los estudios realizados sobre su dieta también indican que ocuparon hábitats muy heterogéneos, que distintas poblaciones muy próximas llegaron a especializar su dieta y que fueron capaces de adaptarse a diferentes altitudes y latitudes donde los ecosistemas son muy diferentes y a los cortos cambios climáticos que transcurrieron durante el Pleistoceno tardío.
El oso de las cavernas en Askondo (Mañaria, Bizkaia)
La cueva de Askondo se encuentra en el término municipal de Mañaria cerca de la ermita de San Lorenzo, en el barrio de Urkuleta. A pesar de que su entrada actual está en parte desmantelada por la cantera Kanterazarra, presenta un desarrollo de 302 m de longitud, y un desnivel total de 9 m. Esta cavidad se desarrolló a favor de un sistema de fracturas de dirección N-S y se formó tanto por disolución durante la etapa freática, como por erosión y desmantelamiento por gravedad durante la etapa vadosa. Esta cueva se desarrolla en calizas arrecifales con rudistas y corales del Cretácico y es parte del sistema kárstico de la unidad hidrogeológica Aramotz.
Las primeras excavaciones tuvieron lugar a comienzos del s. XX por Augusto Gálvez Cañero y posteriormente, la cueva fue visitada por José Miguel de Barandiarán en 1929. En 1963 se recuperaron dos cráneos de oso de las cavernas por parte de Joan Serrés, y durante esta misma década Ernesto Nolte realizó una cata en el interior de la cavidad descubriendo la presencia de restos de carnívoros (mayoritariamente osos) y de humanos y atestigua la destrucción de la entrada por parte de la cantera. Para principios de los años 80 del pasado siglo, la carta arqueológica de Bizkaia señala que es probable que el posible yacimiento arqueológico de la cueva haya sido destruido, tal y como lo están la entrada y parte de la primera sala.
En enero del 2011, una prospección de la cueva, localizó una serie de pinturas rupestres que dio lugar a un proyecto de investigación, financiado por Diputación Foral de Bizkaia-Bizkaiko Foru Aldundia y dirigido por Diego Garate y Joseba Rios-Garaizar, que incluía tres sondeos en distintas zonas del comienzo de la cueva. Estas investigaciones han sido las primeras en dar un contexto arqueo-paleontológico a las ocupaciones de esta cueva por parte de humanos y carnívoros, que evidencian el uso de la cavidad durante distintos momentos de la Prehistoria. Así, la cueva fue ocupada por Neandertales (Homo neanderthalensis) hace más de 45 mil años, y posteriormente por distintos grupos de humanos modernos (Homo sapiens) del Paleolítico Superior: durante el Auriñaciense (hace ~36 mil años, el Gravetiense (hace ~28.500 mil años) y el Solutrense Superior (hace ~20-21 mil años). Por último, durante la Edad del Bronce (hace unos 3.500 años), se depositaron los restos de un niño o una niña de 10 años en esta cueva. En el caso de los osos, además de restos en la superficie de la cueva, sin contexto estratigráfico, los restos recuperados en la excavación en distintos niveles, así como una datación directa por radiocarbono permite proponer que los osos de las cavernas ocuparon la cavidad durante más de 10 mil años. Estos osos usaron Askondo como lugar de hibernación durante distintas generaciones, y en algunas ocasiones, por ser demasiado jóvenes, demasiado viejos o por no haber acumulado suficientes reservas, perecían durante el invierno.
La colección de restos de oso de las cavernas de Askondo depositada en el Hontza Museoa es el fruto de dos donaciones: de una antigua asociación paleontológica del duranguesado, desaparecida hace más de 30 años y de la familia de Unai Periañez.
Más información:
Exposición en Hontza Museoa (hasta septiembre 2020)
Baca, M., Popović, D., Stefaniak, K., Marciszak, A., Urbanowski, M., Nadachowski, A., Mackiewicz, P. (2016) Retreat and extinction of the Late Pleistocene cave bear (Ursus spelaeus sensu lato). The Science of Nature 103, 92.
Garate, D. & Rios, J. (Dir.). La cueva de Askondo (Mañaria, Bizkaia). Arte parietal y ocupación humana durante la Prehistoria. Kobie-Bizkaiko Arkeologi Indusketak, 2. ISBN: (978-)84-7752-470-X; ISSN: 0214-7971.
Gómez-Olivencia, A. (2018). Los macromamíferos continentales de los Pirineos occidentales durante el Pleistoceno: registro fósil, extinciones y nuevas técnicas de estudio. En: Badiola, A., Gómez-Olivencia, A., Pereda Suberbiola, X. (Editores). Registro fósil de los Pirineos occidentales. Bienes de interés paleontológico y geológico. Proyección social. Vitoria-Gasteiz, Servicio Central de Publicaciones del Gobierno Vasco-Eusko Jaurlaritzaren Argitalpen Zerbitzu Nagusia, pp. 179-197. ISBN: 978-84-457-3437-7
Torres Pérez-Hidalgo, Trinidad José (2013). La historia del oso de las cavernas: vida y muerte de un animal desaparecido. Escuela Técnica Superior de Ingenieros de Minas, Madrid.
Torres, T., Nestares, T., Cobo, R., Ortiz, J.E., Cantero, M.A., Ortiz, J., Vidal, R., Prieto, J.O. (2001). Análisis morfológico y métrico de la dentición y metapodios del oso de Deninger (Ursus deningeri , Von Reichenau) de la Cueva Sta. Isabel de Ranero. Aminocronología (Valle de Carranza – Bizkaia – País Vasco). Munibe (Ciencias Naturales – Natur Zientziak) 51, 107-141.
Torres, T., Ortiz, J.E., Fernández, E., Arroyo-Pardo, E., Grün, R., Pérez-González, A. (2014). Aspartic acid racemization as a dating tool for dentine: A reality. Quaternary Geochronology 22, 43-56.
Sobre los autores: Asier Gómez Olivencia (@AsierGOlivencia) es investigador Ramón y Cajal e Ikerbasque Research Fellow en el Departamento de Estratigrafía y Paleontología de la Facultad de Ciencia y Tecnología de la UPV/EHU; Mónica Villalba de Alvarado es investigadora predoctoral en el Centro UCM-ISCIII de Investigación sobre Evolución y Comportamiento Humanos.
El artículo El oso de las cavernas se ha escrito en Cuaderno de Cultura Científica.
Entradas relacionadas:- Sorpresas en la atmósfera del polo sur de Venus
- Artazu VII, una trampa mortal del Pleistoceno que es un tesoro
- Los corredores de élite kenianos oxigenan su cerebro de forma diferente

